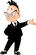I’m looking at the side effects of Madopar, and all of them are listed as «unknown frequency».
How can frequency be unknown? Even if just one of a million patients got a certain side effect, that just means that frequency is 1 millionth, right?
The only reason I can think of, is that zero side effects occurred in the drug’s clinical test, AND people contacted the company about their side effects AFTER the drug was already on the market. That seems unlikely, though.
I found this link but it’s a bit of a wall of text.
asked Apr 24, 2019 at 9:54
0
A GUIDELINE ON SUMMARY OF PRODUCT [pharmaceuticals] CHARACTERISTICS (EUROPEAN COMMISSION, 2009)
In exceptional cases, if a frequency cannot be estimated from the
available data, an additional category frequency ‘not known’ may be
used.
Sometimes, knowing the number of cases of a drug side effects in a certain group of users is not enough to estimate the frequency of side effects in the entire population. For example, if only one person spontaneously reports a side effect, the reported frequency is known, but this may not be enough to estimate the actual frequency, because the producer does not know how many others experienced side effects.
When the reported frequency is low, the producer can’t automatically claim the actual frequency is «low,» so they may say it’s unknown, but you can assume it is probably low, because…when the reported frequency is high, the producer can automatically estimate the actual frequency is also «high.»
answered Apr 25, 2019 at 7:32
JanJan
15.8k22 silver badges70 bronze badges
2
4.8. Нежелательные реакции
В данный раздел включаются все нежелательные реакции, выявленные в ходе клинических исследований, пострегистрационных исследований безопасности и по результатам спонтанных сообщений, в отношении которых причинная связь между лекарственным препаратом и нежелательным явлением после проведения тщательной оценки имеет обоснованную вероятность, и подтверждается, к примеру, их сравнительной частотой возникновения в клинических исследованиях или результатами эпидемиологических исследований и (или) оценкой причины развития на основании сообщений по отдельным случаям. Нежелательные явления, не имеющие по меньшей мере подозреваемую причинную связь, указывать в ОХЛП не следует.
Содержание данного раздела следует обосновать в клиническом обзоре регистрационного досье, основываясь на оценке наиболее убедительных данных в отношении выявленных нежелательных явлений и фактов, значимых для оценки причинно-следственной связи, тяжести и частоты. Данный раздел следует регулярно пересматривать и при необходимости обновлять с целью надлежащего информирования медицинских работников в отношении профиля безопасности препарата. Кроме того, весь раздел может быть пересмотрен при подтверждении регистрации (перерегистрации), когда профиль безопасности большинства препаратов, скорее всего, будет хорошо изучен, и далее при подаче каждого периодического отчета по безопасности (ПООБ).
Информацию следует излагать кратко, используя специальную терминологию, она не должна содержать такие сведения, как указание на отсутствие определенных нежелательных реакций, данные о сравнительной частоте, за исключением указанных ниже, а также указания на общую хорошую переносимость лекарственного препарата, как «хорошо переносится», «нежелательные реакции, как правило, редки» и т.д. Указания на отсутствие подтверждения причинной связи включать не допускается.
В целях представления четкой и понятной информации раздел 4.8 ОХЛП должен иметь следующую структуру:
резюме профиля безопасности;
резюме в форме таблицы нежелательных реакций;
описание отдельных нежелательных реакций;
дети;
прочие особые популяции.
4.8.1. Резюме профиля безопасности.
Резюме профиля безопасности должно содержать сведения о наиболее серьезных и (или) часто возникающих нежелательных реакциях.
При наличии указанных сведений приводятся сроки возникновения нежелательных реакций. Например, в целях предотвращения раннего прекращения терапии может потребоваться описание несерьезных нежелательных реакций, которые часто возникают в начале терапии, но могут разрешиться по мере продолжения лечения, или описание нежелательной реакции, характерной для длительного применения. Частоту приводимых нежелательных реакций следует указать как можно более точно. Резюме профиля безопасности должно соотноситься с важными выявленными рисками, описанными в спецификации по безопасности плана управления рисками. Сведения не должны противоречить резюме в форме таблицы нежелательных реакций. Если в разделе 4.4 ОХЛП приведены значимые меры по минимизации рисков, следует привести ссылку на данный раздел.
Ниже представлен пример возможного указания:
«В начале лечения может возникать эпигастральная боль, тошнота, диарея, головная боль или головокружение; эти реакции, как правило, проходят в течение нескольких дней, даже при продолжении терапии. К наиболее часто возникавшим нежелательным реакциям при лечении относятся головокружение и головная боль, каждая из которых возникала приблизительно у 6% пациентов. Редко может возникать острая печеночная недостаточность и агранулоцитоз (реже чем 1 случай на 1000 пациентов).»
4.8.2. Резюме в форме таблицы нежелательных реакций.
Нежелательные реакции с соответствующей им категорией частоты следует занести в одну таблицу (или структурированный список). В некоторых случаях в отношении частых и очень частых реакций и при необходимости более ясной подачи информации в таблице допустимо привести конкретные значения частоты.
При выраженном различии профилей нежелательных реакций в зависимости от применения препарата, например, в случае применения препарата по разным показаниям (например, в онкологии и по неонкологическому показанию) или при различных режимах дозирования в исключительных случаях допустимы отдельные таблицы.
Перед таблицей необходимо представить сведения об источнике базы данных (например, из клинических исследований, пострегистрационных исследований безопасности или по результатам спонтанных сообщений).
Таблицу следует составлять в соответствии с системно-органной классификацией, представленной в приложении N 4 к настоящим Требованиям. Последовательность представления системно-органных классов должна соответствовать порядку, приведенному в приложении N 4 к настоящим Требованиям. Он, как правило, соответствует уровню предпочтительного термина, однако в некоторых случаях целесообразно указать термин низшего уровня или в исключительных случаях групповые такие термины, как термины высшего уровня. По общему правилу все нежелательные реакции следует отнести к наиболее подходящему системно-органному классу, соответствующему органу-мишени. Например, предпочтительный термин «нарушение функциональных проб печени» следует отнести к системно-органному классу «нарушения со стороны печени и желчевыводящих путей», а не к системно-органному классу «лабораторные и инструментальные данные».
Нежелательные реакции внутри каждого системно-органного класса следует расположить в порядке убывания их серьезности с указанием частоты их возникновения (в рамках одной градации частоты). Наименования, используемые для каждой категории частоты, должны соответствовать стандартным терминам в соответствии со следующим правилом: очень часто ( 1/10), часто (
1/100, но < 1/10), нечасто (
1/1 000, но < 1/100), редко (
1/10 000, но < 1/1 000), очень редко (< 1/10 000).
В исключительных случаях, если на основании имеющихся данных частоту определить невозможно, допускается использовать дополнительную категорию частоты — «частота неизвестна». Если используется выражение «частота неизвестна», в перечень объяснения категорий частоты следует добавить текст «частота неизвестна (на основании имеющихся данных оценить невозможно)». Не следует использовать выражения из отдельных сообщений (единичных случаев).
Если в описании отдельной нежелательной реакции приводятся дополнительные сведения, такую реакцию необходимо выделить, например, с помощью звездочки, а в сноске указать ссылку на соответствующий раздел.
Рекомендации по оценке частоты возникновения нежелательных реакций приводятся в подпункте 4.8.6. настоящих Требований.
4.8.3. Описание отдельных нежелательных реакций.
В данный подраздел следует включить сведения, характеризующие особую нежелательную реакцию, которые могут быть полезны для предотвращения, оценки или купирования возникшей нежелательной реакции в клинической практике.
Указываются сведения, характеризующие отдельные серьезные и (или) часто возникающие нежелательные реакции или те из них, в отношении которых поступали сообщения об их особом течении. Следует представить сведения о частоте (при необходимости с описанием обратимости), времени начала, тяжести, продолжительности, механизме развития (если он клинически значим), зависимости от дозы, продолжительности воздействия лекарственного препарата и факторах риска. Меры, направленные на недопущение развития или принимаемые при развитии определенных нежелательных реакций, следует описывать в разделе 4.4 ОХЛП с указанием ссылки на данный раздел.
Сведения о возникновении реакций синдрома «отмены» допускается представить в данном подразделе вместе со ссылкой на раздел 4.2 ОХЛП (при необходимости постепенного снижения дозы или рекомендации по отмене лекарственного препарата).
Следует описать все различия в профиле нежелательных реакций между различными лекарственными формами.
Следует также включить сведения о комбинированных препаратах, характеризующие нежелательные реакции, обусловленные той или иной фармацевтической комбинацией действующих веществ (при наличии).
Все нежелательные реакции, напрямую обусловленные взаимодействием, следует представить в данном подразделе со ссылкой на раздел 4.5 ОХЛП.
Необходимо также представить сведения о нежелательных реакциях с очень низкой частотой возникновения или с запоздалой манифестацией симптомов, сведения о связи которых с препаратом могут отсутствовать, но которые характерны для лекарственных препаратов того же терапевтического, химического или фармакологического класса. Необходимо указать, что это характеристика класса.
Необходимо описать все нежелательные реакции, обусловленные вспомогательными веществами и производственными примесями.
4.8.4. Дети.
Необходимо во всех случаях предусматривать подраздел по детям (если только он не является незначимым).
Необходимо описать объем и возрастные характеристики базы данных по безопасности у детей (например, данные клинических исследований или данных фармаконадзора). Необходимо указать на неопределенность имеющихся данных вследствие их ограниченности.
Если выявленный профиль безопасности у детей и взрослых совпадает, допускается привести текст: «Частота, вид и тяжесть нежелательных реакций у детей и взрослых [одинаковы, ожидается, что будут одинаковы]». Аналогично надлежит указать, имеются ли различия в профилях безопасности в различных возрастных группах детей.
Все клинически значимые различия (т.е. по характеру, частоте, серьезности и обратимости нежелательных реакций) в профиле безопасности у взрослых и детей, а также между различными возрастными группами детей необходимо описать и представить по каждой возрастной группе. При необходимости специального мониторинга следует дать ссылку на раздел 4.4 ОХЛП. Для клинически значимых различий можно представить отдельное резюме в форме таблицы нежелательных реакций по частоте по соответствующим возрастным группам сообразно обстоятельствам. Если некоторые нежелательные реакции у детей являются частыми ( 1/100, но < 1/10) или очень частыми (
1/10), в скобках необходимо указать частоту. При наличии больших различий в профиле безопасности по сравнению со взрослыми с целью удобочитаемости информации допускается привести резюме профиля безопасности у детей. Необходимо также обобщить имеющиеся сведения из всех достоверных научных источников о долгосрочной безопасности у детей (например, в отношении роста, умственного развития и полового созревания) со ссылкой на раздел 5.1 ОХЛП, если применимо. Необходимо оговорить все факторы риска (например, продолжительность терапии или период наступления риска).
Симптомы синдрома «отмены» у новорожденных (если значимо) следует перечислить в отдельном абзаце со ссылкой на раздел 4.6 ОХЛП.
4.8.5. Прочие особые популяции.
Данный раздел может содержать сведения о каких-либо клинически значимых различиях (например, по характеру, частоте, серьезности и необратимости нежелательных реакций, а также о необходимости мониторинга), выявленных в других особых группах (например, как пожилые, пациенты с почечной недостаточностью, пациенты с печеночной недостаточностью, пациенты с другими заболеваниями или с определенным генотипом). При необходимости допускается привести ссылки на другие разделы ОХЛП, например, 4.3, 4.4 или 4.5.
Причиной возникновения нежелательных реакций может быть также генетически обусловленный метаболизм препарата. У субъектов и пациентов с дефицитом определенного фермента частота и тяжесть нежелательных реакций может быть другой. На это необходимо указать и, если значимо, соотнести с данными клинических исследований.
4.8.6. Дополнительные рекомендации по оценке частоты возникновения нежелательных реакций.
Оценка частоты возникновения нежелательных реакций зависит от источника данных (например, клиническое исследование, пострегистрационное исследование безопасности или спонтанное сообщение), качества сбора данных и оценки причинно-следственной связи. Если выбор категории частоты основывается на разных источниках, следует выбрать категорию, отражающую наибольшую частоту возникновения, если только не использовался более специфичный метод, в связи с чем полученная оценка обладает явно более высокой валидностью, например, объединенный анализ подходящих исследований.
Источником данных должна служить популяция, подвергшаяся воздействию лекарственного препарата в дозах и с продолжительностью лечения, рекомендованных ОХЛП.
Реакции, которые в сообщениях обозначались различными терминами, но представляющие собой одно и то же явление (например, вялость, сонливость, дремота), следует, как правило, объединить в одну нежелательную реакцию, чтобы избежать эффекта «размывания» истинного смысла явления. Аналогично реакции, представляющие собой синдромо-комплекс, следует, как правило, группировать под соответствующим заголовком, чтобы избежать «размывания» его смысла вследствие многообразия составляющих его симптомов.
4.8.7. Нежелательные реакции, выявленные в клинических исследованиях.
В целях повышения точности при установлении частоты возникновения нежелательных реакций необходимо объединить данные по безопасности нескольких исследований без привнесения систематических ошибок (например, существенные различия между характеристиками популяций или экспозиции).
Частоту возникновения нежелательных реакций следует определять, объединив данные плацебо-контролируемых исследований (при наличии таких данных), при этом базы данных должны быть достаточно объемными, чтобы быть информативными. При отсутствии этих данных или недостаточной их информативности для оценки частоты можно воспользоваться базами данных активно-контролируемых, или не сравнительных или дополнительных (add-on) исследований.
Частота должна отражать общую частоту возникновения (а не разницу или относительные риски по отношению к плацебо или другому контролю).
Если частая, очень частая или серьезная нежелательная реакция (например, суицид) также возникает в группе плацебо со значимой частотой, допускается указать обе частоты возникновения, чтобы лучше охарактеризовать риск (например, в подразделе с описанием отдельных нежелательных реакций).
4.8.8. Нежелательные реакции, выявленные при проведении исследований по безопасности.
Выбор категории частоты возникновения, которая будет присвоена каждой нежелательной реакции, основывается на точечной оценке общей частоты возникновения, рассчитанной по результатам исследования, спланированного таким образом, чтобы отдельные нежелательные явления, возникающие у пациентов в заданный период наблюдения, могли быть выявлены и отнесены к применению лекарственного препарата. В этой ситуации допускается рассчитать точечную оценку общей частоты возникновения с использованием стандартных статистических методов. Если исходная информация выражена в виде плотности частоты возникновения (знаменатель выражен в единицах «человек — время», например, «пациенто-лет», «пациенто-дней»), для выбора категории частоты возникновения необходимо провести надлежащее преобразование в отношение (пропорцию) частоты возникновения. В норме для определения категории частоты возникновения следует использовать отношения частоты возникновения наиболее репрезентативного периода воздействия лекарственного препарата (например, 1 неделя, 3 месяца, 1 год). Однако это невозможно, если вредность применения лекарственного препарата увеличивается со временем. В этом случае нежелательную реакцию и характер частоты ее возникновения, если они клинически значимы, следует должным образом описать в разделе с описанием отдельных нежелательных реакций.
Категория частоты возникновения, присваиваемая каждой нежелательной реакции должна основываться на разнице с контролем. Если данные получены из исследования с участием группы, не подвергшейся воздействию лекарственного препарата, а разница в частоте возникновения, отнесенная к применению лекарственного препарата, меньше исходной или фоновой частоты возникновения, при этом нежелательная реакция является важной, допускается указать фоновую частоту возникновения (например, в разделе с описанием отдельных нежелательных реакций).
4.8.9. Нежелательные реакции по результатам спонтанных сообщений.
Число спонтанных сообщений указывать не следует, поскольку эти данные могут быстро устаревать. Частоту возникновения, основанную на количестве сообщений, извлеченных из системы сбора спонтанных сообщений, для определения категории частоты возникновения использовать не следует. Если с помощью спонтанных сообщений выявлена неожиданная нежелательная реакция, в целях определения категории частоты возникновения необходимо проанализировать каждое надлежащим образом спланированное исследование, в котором могла быть выявлена данная реакция. Если нежелательная реакция в клинических исследованиях никогда не возникала, тогда верхняя граница 95-процентного интервала не превышает 3/X, где X — общий размер выборки во всех значимых клинических исследованиях (например, с длительным периодом последующего наблюдения, достаточным для обнаружения этой нежелательной реакции). Например, если определенная нежелательная реакция у 3600 субъектов, подвергшихся воздействию лекарственного препарата в клинических исследованиях, не выявлялась, то верхняя граница 95-процентного доверительного интервала для точечной оценки 1/1 200, что соответствует категории «редко» — при принятии худшего значения точечной оценки. Основания выбора категории частоты такой реакции можно привести в разделе с описанием отдельных нежелательных реакций.
О стандартах медицинской помощи
Министерством здравоохранения и социального развития Российской Федерации (МЗ и СР РФ) разработан набор стандартов оказания амбулаторно-поликлинической и санаторно-курортной помощи больным с различными заболеваниями.
Эти стандарты представляют собой формализованное описание (в табличной форме) минимально необходимого объема медицинской помощи, которая должна быть оказана пациенту с конкретной нозологической формой (заболеванием), синдромом или в конкретной клинической ситуации. Работа по их созданию была инициирована в связи с необходимостью нормативно-правового обеспечения оказания дополнительной бесплатной медицинской помощи гражданам, имеющим право на набор социальных льгот. Основными задачами при разработке этих стандартов были:
— обоснование Перечня лекарственных средств, отпускаемых по рецептам врача (фельдшера) при оказании дополнительной бесплатной медицинской помощи отдельным категориям граждан, имеющим право на получение государственной социальной помощи;
— определение объемов медицинской помощи (перечней работ и услуг, лекарственных средств) для расчета затрат на ее оказание.
К настоящему моменту определены объемы медицинской помощи по наиболее значимым заболеваниям для амбулаторно-поликлинических условий. В то же время не удалось избежать расхождений требований стандартов (в части лекарственной терапии) с утвержденным Перечнем лекарственных средств, в частности из-за сложности достижения консенсуса между участниками процесса согласования нормативных документов, и в этом направлении еще предстоит большая работа.
Приоритетный перечень заболеваний (групп заболеваний, синдромов), по которым необходимо в первую очередь разработать стандарты, сформирован на основании анализа государственной отчетности о состоянии здоровья населения и включает заболевания, представляющие собой наиболее значимые медико-социальные проблемы (высокая или быстро увеличивающаяся распространенность, существенная доля в структуре причин смерти и выхода на инвалидность).
Утвержденные на настоящем этапе стандарты распространяются на оказание помощи только в амбулаторно-поликлинических и санаторно-курортных условиях.
Стандарты разработаны с привлечением экспертов-специалистов из ведущих медицинских учреждений: Московской медицинской академии им. И.М. Сеченова, Московского государственного медико-стоматологического университета, Кардиологического научного центра МЗ и СР РФ, Научного центра акушерства, гинекологии и перинатологии РАМН, Центра микрохирургии глаза, НИИ ревматологии РАМН, Эндокринологического научного центра РАМН и др.
Для разработки стандартов были использованы утвержденные МЗ РФ Протоколы ведения больных и подготовленные к утверждению проекты протоколов, разработанные экспертами-специалистами в различных областях медицины. В дополнение к протоколам ведения больных в качестве источников информации о целесообразности применения отдельных медицинских услуг и лекарственных средств в конкретных клинических ситуациях были использованы Федеральное руководство для врачей по использованию лекарственных средств, Государственный реестр лекарственных средств, ежегодный справочник «Доказательнаямедицина» (М., Медиа-Сфера), а также монографии по отдельным направлениям медицины.
Структура стандарта
Каждый стандарт начинается с модели пациента, который подлежит ведению согласно представленному плану. Модель включает основные характеристики пациента, определяющие тактику диагностики и лечения:
— наименование нозологической формы или синдрома;
— соответствующий код по МКБ-10;
— фаза заболевания и стадия (если необходимо);
— осложнения (или их отсутствие).
Стандарт может включать как одну, так и несколько моделей.
Для каждой модели пациента определены условия оказания (амбулаторно, в стационаре) и функциональное назначение (диагностика, профилактика, лечение, реабилитация) медицинской помощи с перечнем:
1) медицинских работ и услуг для диагностики заболевания;
2) медицинских работ и услуг для лечения заболевания;
3) групп и международных непатентованных наименований (МНН) лекарственных средств для лечения заболевания.
В перечнях диагностических и лечебных работ и услуг указаны:
— код медицинской работы (услуги) согласно Номенклатуре работ и услуг в здравоохранении;
— наименование медицинской работы (услуги) согласно Номенклатуре работ и услуг в здравоохранении;
— частота предоставления работы (услуги) в группе пациентов, подлежащих ведению по данному плану;
— кратность оказания услуги каждому пациенту.
В стандарте могут быть указаны как простые медицинские услуги (например, измерение массы тела, определение содержания белка в моче), так и сложные и комплексные — например, первичный прием (осмотр, консультация) врачом-невропатологом. Состав сложных и комплексных медицинских услуг расшифрован в соответствующем разделе Номенклатуры работ и услуг в здравоохранении.
Частота предоставления услуги в группе пациентов, подлежащих ведению по данному плану, отражает вероятность выполнения медицинской работы (услуги) для данной модели пациента на 100 человек и может принимать значения от 0 до 1, где 1 означает, что всем 100% пациентов, соответствующих данной модели, необходимо оказать данную услугу. Цифры менее 1 означают, что настоящая услуга оказывается не всем пациентам, а лишь при наличии соответствующих показаний и возможности оказания подобной услуги в конкретном учреждении. Так, показатель 0,1 означает, что данная услуга предоставляется в среднем 10% пациентов; показатель 0,5 — 50% пациентов и т. д.
Частота предоставления услуги определена экспертами-разработчиками с учетом доказательств ее эффективности, безопасности и экономической целесообразности, а также собственного опыта практической работы. Приведем пример.
Приказом МЗ и СР РФ № 77 от 13.08,04 утвержден стандарт медицинской помощи пациентам с ВИЧ-инфекцией. В стандарте представлены 2 модели пациента. В модели 1 в табл. 1.1 дан перечень медицинских работ и услуг, функциональное назначение которых — диагностика:
— Услуга А01.31.001. Сбор жалоб и анамнеза при инфекционном заболевании: частота предоставления — 1 (все 100% пациентов получают данную услугу), среднее количество — 1 (однократно на этапе диагностики).
Та же модель, перечень медицинских работ и услуг, функциональное назначение — лечение в расчете на 1 год:
— Услуга А09.05.003. Исследование уровня общего гемоглобина в крови: частота предоставления — 1 (все 100% пациентов получают данную услугу), среднее количество — 4 (каждый пациент получает данную услугу в среднем 4 раза за год лечения). Далее приводится перечень групп и МНН лекарственных средств для лечения, при этом указываются:
— фармако-терапевтические группы лекарственных средств, которые должны быть назначены пациентам, соответствующим данной модели (например, «Средства для лечения и профилактики инфекций»);
— группы лекарственных средств согласно анатомо- те-рапевтическо-химической (АТХ) классификации (например, противовирусные средства);
— МНН лекарственных средств.
Для всех 3 групп указана частота назначения лекарственных средств пациентам, соответствующим данной модели, а для МНН также:
• ориентировочная дневная доза (ОДД);
• эквивалентная курсовая доза (ЭКД).
ОДД определялась в соответствии с рекомендациями клинических протоколов ведения больных или Федерального руководства для врачей по использованию лекарственных средств. Представленная в стандартах ОДД является средней рекомендуемой дозой, которая главным образом должна использоваться для расчета необходимых на лекарственную терапию затрат. Она не отражает форму выпуска лекарственных средств и особенности их применения (возрастные различия в дозировках, титрование дозы и т.п.) и не предназначена для непосредственного использования врачом при назначении лекарства больному.
При оказании медицинской помощи врачи назначают лекарственные средства в дозах, рекомендованных инструкциями по их применению, алгоритмами медикаментозной терапии, описанными в протоколах ведения больных и иных нормативных документах и источниках информации, с учетом особенностей состояния здоровья и течения заболевания у конкретного больного.
ЭКД равна количеству дней назначения лекарственного средства, умноженному на ОДД. Частота назначения, как и в перечне медицинских работ и услуг, может принимать значения от 0 до 1, где 1 означает, что 100% пациентов, соответствующих данной модели, должны получать лекарственные средства данной фармако-терапевтической или АТХ-группы.
В стандарте медицинской помощи больным ВИЧ-инфекцией указано:
Фармако-терапевтическая группа «Средства для лечения и профилактики инфекций» — частота назначения 1,0 (все пациенты, соответствующие данной модели).
Из средств для лечения и профилактики инфекций больные получают противовирусные средства — частота назначения 1,0(100%).
Перечень противовирусных средств состоит из 15 МНН, например:
Зидовудин — частота назначения 0,3 (30%); ОДД — 0,6 г; ЭКД из расчета 1 год — 219,0 г (0,6 г х 365 дней). Сумма частоты назначения МНН внутри группы равна 1 (100%), если предполагается, что больному назначается только одно из альтернативных МНН, исходя из требований протоколов ведения больных, доступности лекарств, формулярного перечня территории или учреждения, других факторов. Если необходима комбинированная терапия (одновременно 2 и более препаратов внутри АТХ-группы), частота назначения МНН внутри группы соответственно больше 1.
Применение стандартов
Стандарт медицинской помощи в амбулаторно-поликлинических и санаторно-курортных условиях определяет рекомендуемый перечень медицинских услуг и лекарственных средств (по МНН).
Врач должен обеспечить пациенту, соответствующему условиям представленных моделей, получение медицинских работ и услуг, а также лекарственных средств из указанных в стандарте перечней.
Назначение медицинских услуг
Если напротив наименования услуги (лекарственного средства) указана частота 1 (100%), назначение этой услуги (лекарственного средства) показано всем пациентам независимо от особенностей течения заболевания при отсутствии у них противопоказаний.
Если напротив наименования услуги (лекарственного средства) указана частота менее 1, врач решает вопрос о необходимости ее применения индивидуально, учитывая рекомендации протоколов ведения больных, особенности течения заболевания у конкретного пациента и возможности медицинского учреждения. В среднем частота назначения услуг (лекарственных средств) в группе пациентов, соответствующих условиям модели, должна приближаться к указанной в стандарте.
Если у пациента уже установлен окончательный диагноз, он получает лечебные медицинские услуги и лекарственные средства (диагностические услуги ему могут не оказываться, если нет необходимости в уточнении диагноза). Если диагноз окончательно не установлен, а только предполагается, медицинская помощь пациенту включает диагностические медицинские услуги (в соответствии с диагностической гипотезой), а после установления диагноза — лечебные услуги и назначение лекарственных средств. В части стандартов диагностическая модель выделяется отдельно.
Назначение лекарственных средств
Если напротив наименования группы лекарственных средств указана частота 1 (100%), назначение препаратов из этой группы показано всем пациентам при отсутствии у них противопоказаний.
Если напротив наименования группы указана частота менее 1, врач решает вопрос о необходимости ее применения индивидуально с учетом рекомендации протоколов ведения больных, особенностей течения заболевания у конкретного пациента и возможностей медицинского учреждения. С учетом тех же факторов врач выбирает из предложенных внутри одной группы МНН конкретное лекарственное средство для конкретного пациента и затем самостоятельно выбирает торговое наименование (лекарственный препарат), исходя из доступности препарата, формулярного перечня территории или учреждения или других факторов.
В среднем частота назначения лекарственных средств в группе пациентов, соответствующих условиям модели, должна приближаться к указанной в стандартах.
Стандарт позволяет назначать пациенту комбинированную терапию (если комбинируются препараты из одной группы, суммарная частота их применения превышает 1,0).
При наличии у пациента сопутствующих заболеваний лечение каждого из них осуществляется в соответствии со своим стандартом. При этом нет необходимости суммировать диагностические или лечебные услуги, которые имеются одновременно в нескольких стандартах. Кратность оказания услуг, присутствующих одновременно в нескольких стандартах, должна составлять максимальную величину из указанных в различных стандартах.
Так, если в одном стандарте указано, что общий анализ мочи проводится за период лечения однократно, а в другом — 3
раза, то больной должен получить эту услугу 3 раза.
Решая вопрос о назначении лекарственных средств, врач должен действовать в соответствии с принципами рациональной фармакотерапии и учитывать вероятность лекарственных взаимодействий.
При развитии осложнения, изменении диагноза в ходе наблюдения тактика ведения пациента должна быть изменена и приведена в соответствие с новым стандартом или моделью пациента.
Использование стандартов при оказании дополнительной бесплатной медицинской помощи гражданам, имеющим право на получение набора социальных услуг. Стандарты медицинской помощи рекомендуются для использования при оказании дополнительной бесплатной медицинской помощи гражданам, имеющим право на получение набора социальных услуг.
Участковый терапевт, участковый педиатр, врач общей практики (семейный врач), фельдшер оказывают помощь в соответствии с утвержденными стандартами, пользуясь рекомендациями по их применению, представленными в нормативных документах: Приказах МЗ и СР № 255 от 22.11.04 «О порядке оказания первичной медико-санитарной помощи гражданам, имеющим право на получение набора социальных услуг», № 256 от 22.11.04 «О порядке медицинского отбора и направления больных на санаторно-курортное лечение», № 26-МЗ от 25.01.2005 г. «Об организации работы по медицинскому обеспечению отдельных категорий граждан, получателей набора социальных услуг».
При необходимости (наличии показаний) пациентам могут назначаться услуги и лекарственные средства, не включенные в настоящие стандарты.В соответствии с Письмом МЗ и СР России № 26-МЗ от 25.01.05 «Об организации работы по медицинскому обеспечению отдельных категорий граждан, получателей набора социальных услуг» оплате за счет средств Федерального бюджета подлежат:
• лекарственные средства в соответствии с «Перечнем лекарственных средств», утвержденным приказом МЗ и СР РФ от 02.12.04 г. №296;
• лекарственные средства, назначенные по решению врачебной комиссии в соответствии с приказом МЗ и СР РФ от 24.12.04 №321.
При ведении больного с заболеваниями, по которым стандарты в настоящее время не утверждены, врач принимает решение самостоятельно, исходя из собственных знаний и опыта.
Важным условием эффективного использования стандартов в практическом здравоохранении является мониторирование процесса их использования, предполагающее сбор замечаний и предложений от медицинских учреждений, их обобщение и при необходимости внесение соответствующих коррективов в содержание.
В настоящее время формируется 3-уровневая система нормативных документов, регламентирующих оказание медицинской помощи больным: протоколы ведения больных на национальном (федеральном) уровне; клинико-экономические протоколы на уровне региона и муниципального образования, клинические протоколы медицинской организации.
Утвержденные стандарты медицинской помощи формируют нормативно-правовое обеспечение на промежуточном этапе становления данной системы.
Предполагается, что по мере формирования многоуровневой системы требования этих стандартов будут пересмотрены, а сами стандарты станут частью протоколов ведения больных с соответствующими заболеваниями.
Осложнения лекарственной терапии называют по-разному: побочным действием препаратов, лекарственной аллергией, непереносимостью препарата, лекарственной патологией т.п.
- Группы побочных действий препаратов
- Частота возникновения побочных действий препаратов
- Классификация побочных действий препаратов
- Причины побочных действий препаратов
- Виды побочных действий препаратов
- Значение плацебо в определении эффективности и побочных действий препаратов
Нежелательные реакции, которые вызываются некоторыми лекарственными средствами, можно объединить понятием «побочное действие препарата» или «осложнения фармакотерапии».
Группы побочных действий препаратов
В клинико-фармакологическом аспекте побочные действия препаратов целесообразно разделить на несколько групп.
Аллергические реакции негативного и замедленного типа чаще всего вызывают препараты:
- золота — 30-40%;
- пенициллин -5-55%;
- противотуберкулезные средства — 8-45% и другие.
Клинически они проявляются:
- дерматитом — в 45-50% случаев;
- эозинофилией — 40-45%;
- лейкоцитозом — 20-30%;
- лейкопенией — 15-25%;
- крапивницей — 10-20% и др.
Такие клинические явления обусловлены аллергизацией организма больных, а также качеством препаратов (технология изготовления, длительность и условия хранения). Так, тетрациклины редко вызывают аллергические реакции, из-за неправильного хранения и приема препарата с пролонгированным сроком хранения это средство может вызвать активную аллергическую реакцию (О.П.Викторов, 2008).
Фармакотоксические реакции обусловлены абсолютной или относительной передозировкой препарата, проявляюется симптомами, обусловленными фармакодинамическими свойствами веществ (атропин — сухость во рту; резерпин — невролептичний эффект у больных гипертензивной болезнью). Клинически это язвенные поражения слизистой оболочки пищеварительного канала, изменение количества клеток крови, нарушение функций паренхиматозных органов и т.д. Возможны проявления неспецифических свойств препарата, в частности влияние на плод во время беременности (эмбриотоксичность, тератогенный эффект, фетотоксичность), а также канцерогенное, мутагенное действия.
Изменение иммунобиологических свойств организма (ослабление иммунных реакций — иммуносупрессия, проявляющаяся суперинфекцией, частыми рецидивами инфекционных заболеваний, дисбактериозом, кандидозом, стафилококковым поражением кожи и других органов). Такие осложнения вызывают:
- антибиотики,
- сульфаниламиды,
- иммунодепрессанты,
- противоопухолевые средства.
Частота возникновения побочных действий препаратов
Вопросу о побочном и токсическое действие препаратов посвящено немало крупных монографий как в нашей стране, так и за рубежом, написано много информационных писем об осложнениях лекарственной терапии. Эти письма составлены на основе сообщений из лечебных учреждений о различных видах побочных действий препаратов.
Анализ полученного материала показал, что самую многочисленную группу препаратов, применение которых вызвало побочные действия, составляют противомикробные и противопаразитарные средства (45,1-43,7%). Значительную группу лекарственных осложнений вызывают стероидные гормоны, анальгезирующие, жаропонижающие и противовоспалительные средства.
К 1968 в английской литературе сообщалось о появлении различных отрицательных реакций при медикаментозном лечении в среднем у 15% людей. Но уже к 1972 году американские авторы наблюдали отрицательные реакции при медикаментозной терапии у 55% человек.
Происходит постоянное увеличение смертельных случаев при введении пенициллина. Во Франции за последние годы частота смертельных случаев при введении пенициллина возросла в 16 раз. Возникает естественный вопрос: наблюдались ли негативные действия лекарств в предыдущие периоды развития медицины?
Уже во времена Гиппократа было известно, что лекарственные средства при одних обстоятельствах обеспечивают желаемое лечебное действие, а при других — вызывают нежелательные эффекты, которые ухудшают здоровье человека. В 1881 году в Берлине Левин выпустил книгу «Побочное действие препаратов». В восьмидесятые и девяностые годы XIX века врачи начали производить противопоказания для назначения медикаментов. К концу XIX века у врачей сложилось убеждение о необходимости подбора соответствующих лекарств в соответствующей дозе для данного конкретного человека.
Классификация побочных действий препаратов
На сегодняшний день не существует точной классификации побочный действий / побочных реакций препаратов. В 1967 было принято классификацию нежелательного действия лекарственных средств.
- Передозировка:
- абсолютная,
- относительная.
- Непереносимость.
- Побочные действия:
- специфические,
- неспецифические.
- Вторичное действие.
- Идиосинкразия.
- Аллергические реакции.
Тареев А.Н. (1968г.) предложил схему этиологических и патогенетических факторов лекарственного синдрома: токсические, неспецифические, тератогенные и мутагенные. Такая классификация проявлений побочного действия препаратов раскрывает генез отдельных его синдромов и тем самым определяет соответствующее патогенетическое лечение.
По механизмам возникновения несовместимости организма с лекарством выделяются:
- медикаментозная аллергия,
- лекарственная токсичность,
- медикаментозная идиосинкразия.
Токсические эффекты — результат применения лекарств в высоких дозах. Идиосинкразия — генетически обусловленная реакция организма. Лекарственная аллергия определяется иммунологическими факторами организма и препарата.
ВОЗ выделяет следующие основные группы побочных реакций:
- Аллергические, не зависящие от дозы препарат, — тип В.
- Токсичные, зависящие от дозы препарата, — тип А.
- Местные — в местах введения.
- Реакции при взаимодействии препаратов — возникают при применении нескольких лекарственных средств и является следствием их взаимовлияния на процессы фармакокинетики и / или фармакодинамики.
- Реакции в отличия препаратов.
- Тератогенные эффекты — аномалии развития плода, связанные с применением препаратов.
- Канцерогенные эффекты — образование опухолей, связано с применением лекарственных средств.
Причины побочных действий препаратов
Побочное действие препарата — это любая нежелательная реакция, обусловленная фармакологическими свойствами лекарственного средства, которая наблюдается исключительно при применении в дозах, рекомендованных для медицинского применения. Побочная реакция препарата — это совокупность или отдельные проявления негативных свойств лекарственного средства, которые препятствуют его эффективному и безопасному применению у пациента или вызывают негативное влияние на качество его жизни. Побочная реакция является непреднамеренной и вредной для организма реакцией, которая возникает при применении препарата в терапевтических дозах с целью профилактики, лечения, диагностики заболевания, модификации физиологической функции. Прием лекарственного средства всегда связан с определенным риском.
Причины же неизбежного риска, как считают Д. Лоуренс, П. Бенитт (1991), при проведении фармакотерапии заключаются в следующем:
- Недостаточная селективность действия лекарственного средства.
- Некоторые эффекты лекарств, желаемые в одной системе организма, могут вызвать нежелательный эффект в других.
- В реализации многих физиологических функций участвуют близкие аналогичные механизмы.
- Длительное воздействие на клеточные механизмы могут привести к постоянным изменениям структуры и функции клеток (в том числе и канцерогенеза).
- Ограниченность информации о патологических процессах.
- Больные генетическими болезнями могут пострадать в очень высокой степени, у них может возникнуть непредвиденный иммунный ответ на введение лекарственного вещества.
- Подбор необходимой дозы неизбежно неточен (сахарный диабет, депрессия).
- В случаях некомпетентного и случайного назначения лекарств.
Виды побочных действий препаратов
Различают явные или очевидные побочные действия препаратов с определенной клинической характеристикой (АГ при длительном употреблении ГКС) и редкие и непредсказуемые (не описаны в литературе и, возможно, не всегда связаны с действием препарата).
По клиническому течению различают:
- легкие — без отмены препарата или специального лечения (головная боль при употреблении нитратов);
- умеренные, которые требуют отмены препарата и назначения лечения (крапивница);
- тяжелые — с угрозой для жизни или инвалидизации пациента (анафилактический шок);
- смертельные.
Поэтому побочные действия препаратов делят на серьезные и несерьезные.
Серьезные побочные действия препаратов — это такие, которые создают угрозу жизни (независимо от дозы), приводят к смерти больного, утраты трудоспособности, требуют дополнительной госпитализации, способствуют аномалии развития плода или врожденным аномалиям, происходящие вследствие передозировки лекарств. Разница между серьезными и тяжелыми побочными явлениями заключается в том, что серьезные — предусматривают значительный вред для здоровья больного вследствие развития эффектов, которые указаны выше, а тяжелые — это мера проявления побочных явлений.
Несерьезные побочные действия препаратов определяется как любая из побочных реакций, которая не соответствует критериям, имеющим отношение к «Серьезным побочных реакциям».
Побочные действия препаратов являются предсказуемыми и непредсказуемыми.
Предполагаемые побочные реакции описаны в общеизвестных справочниках, руководствах, учебниках, монографиях, а также листках- вкладышах (инструкциях по применению лекарственных средств). Развитие ожидаемой побочный реакции не может быть причиной для судебного дела против врача.
Непредсказуемая побочная реакция (по характеру, тяжести течения или частотой возникновения) не ожидается, не описана в общеизвестных справочниках, руководствах, учебниках, монографиях, руководствах для медицинского назначения.
Следует отличать еще и побочный эффект — реакцию, не связанную с терапевтической целью, безвредную или такую, что вредит, действие лекарственного препарата в терапевтических дозах, оказывается рядом с основной специфическим действием (сонливость при введении блокаторов рецепторов гистамина Н1 первой генерации).
К возникновению побочных действий препарата приводят склонность назначения лекарств в высоких терапевтических концентрациях, назначение лечения в дозах без учета индивидуальных особенностей больного, его наследственности, длительное лечение, детский и пожилой возраст пациентов, а также полипрагмазия.
После установления связи между желаемым фармакологическим и побочным эффектом возникает необходимость дать количественную и качественную оценку соотношения польза / риск, то есть, — вероятность того, обнаруженный побочный эффект будет ухудшать течение заболевания и эффективность лечения.
При приеме препарата возможно возникновение нежелательных «феноменов» — синдрома отмены («рикошета»), толерантности к терапии, лекарственной зависимости и т.д. Синдром отмены возникает при внезапном прекращении приеме препарата (отмена клофелина и гипертонический криз, антиангинальные средства — приступ стенокардии). Толерантность к терапии тяжело отличить от пониженной чувствительности пациента к препарату и только тогда можно думать о ней, когда отсутствие эффекта от применения лекарства нельзя преодолеть увеличением дозы или эффект проявляется в дозе, вызывающей нежелательные, опасные эффекты.
Длительное повторное, не всегда регулярное, введения лекарств, которые изменяют психические функции (психостимуляторы или обезболивающие, подавляя ЦНС), может привести к развитию лекарственной зависимости, которая может быть психической (с неудержимым влечением больного и расстройствами психики) и физической (с тяжелыми нарушениями функций внутренних органов и развитием абстиненции).
Значение плацебо в определении эффективности и побочных действий препаратов
Для проверки терапевтической эффективности лекарственных средств при клинических испытаниях используют препараты-«пустышки» — плацебо. Плацебо — этот термин, узаконенный медициной в 1894 году, обозначает препарат, который заведомо не обладает никакими целебными свойствами. Первоначально это были «таблетки» из сахарной пудры или другого приятного на вкус вещества. Латинское слово «плацебо» и переводится дословно как «нравлюсь». Феномен плацебо заключается в том, что оно показывает удивительные (в сравнении со своими нулевыми целебными качествами) результаты.
Масштабные исследования, проведенные в 1986 году под эгидой Министерства социальной защиты Франции, показали: после приема плацебо головные боли проходят в 62% случаев, язвы и гастриты бесследно исчезают у 58 пациентов из ста, каждый второй излечивает ревматизм … Для этого необходимо одно — обмануть больного, сказав, что ему дают настоящее лекарство. Специалисты считают, что секрет плацебо кроется в самовнушении. Но эта гипотеза не объясняет многих странностей эффекта плацебо, например, его географической избирательности. Эксперименты показали, что на разных географических широтах процент успешного действия может отличаться достаточно резко. Это не укладывается ни в одно из объяснений и свидетельствует о том, что феномен плацебо еще далек от его полного понимания специалистами.
Плацебо неспособно действовать непосредственно на те условия, ради изменения которых выписывают препарат. Кроме того, сроком эффекта плацебо называют само явление немедикаментозного действия, не только препарата, а, например, облучения (иногда используют разные «мигающие» аппараты, «лазеротерапию» и др.). Как вещество для плацебо часто используют лактозу. Степень проявления плацебо-эффекта зависит от внушаемости человека и внешних обстоятельств «лечения», например, от размера и яркого цвета таблетки, степени доверия врачу, авторитета клиники.
Используется плацебо как контрольный препарат в клинических испытаниях новых лекарственных препаратов, в процедуре количественной оценки эффективности лекарств. Одной группе испытуемых дают тестируемый препарат, проверенный на животных, а другой — плацебо. Эффект от применения препарата должен достоверно превышать эффект плацебо, чтобы препарат признать действующим. Плацебо используется также для изучения роли самовнушения в действии лекарственных препаратов.
Типичный уровень положительного плацебо-эффекта в плацебо-контролируемых клинических испытаниях в среднем составляет 5-10%, при этом его выраженность зависит от вида заболевания. В большинстве испытаний проявляется и отрицательный плацебо-эффект (эффект ноцебо): 1-5% пациентов испытывают те или иные формы дискомфорта от приема «пустышки» (аллергия, желудочные, сердечные проявления). У некоторых людей неприятные ожидания от нового лекарства могут принять форму выраженной фармакофобии или фармакофилии.
Иногда врачи намеренно прописывают плацебо пациентам, склонным к самовнушению болезненных ощущений. В этом случае появляется возможность избежать неоправданных, типичных для людей в современном обществе неврозов и многочисленных медикаментозных осложнений. Положительный эффект гомеопатических средств также объясняется эффектом плацебо.
Многие современные лекарственные препараты действуют интегрально, их лечебный эффект содержит и «плацебо-составляющую». Поэтому яркие и крупные таблетки в целом действуют сильнее мелких и невзрачных, а препараты известных фирм (и того же состава, и той же биоэквивалентности) дают больший эффект, чем препараты «аутсайдеров рынка».
Это лечебное внушение, не требует каких-либо специальных навыков, поскольку критичность сознания («не верю») преодолевается путем привязки информации, внушается, до фактического объекта — таблетки или инъекции без какой-либо реального действия на организм. Пациента сообщают, что данный препарат обладает определенным действием на организм, и, несмотря на неэффективность препарата, ожидаемое действие проявляется в той или иной степени. Физиологически это связано с тем, что, в результате внушения, мозг пациента начинает выработку соответствующих этому действию веществ, в частности эндорфинов, которые, по сути, частично заменяют действие препарата.
Второй фактор, обеспечивающий эффективность плацебо, — повышение «защитных сил» человека. Степень проявления эффекта плацебо зависит от уровня внушаемости человека и физиологической возможности образования необходимых химических соединений.
Активное вещество: цетиризина дигидрохлорид 10 мг/мл;
вспомогательные вещества: пропиленгликоль (Е1520), глицерин, натрия ацетат тригидрат, сахарин натрий (Е954), метилпарагидроксибензоат (Е218), пропилпарагидроксибензоат (Е216), уксусная кислота ледяная, вода очищенная.
Антигистаминное средство для системного применения, производное пиперазина.
Код АТС: К06АЕ07
Цетиризин, метаболит гидроксизина, является мощным селективным антагонистом периферических гистаминовых Н1-рецепторов, оказывает антигистаминное, противоаллергическое действие. Предупреждает развитие и облегчает течение аллергических реакций, обладает противозудным и антиэкссудативным действием. Влияет на раннюю стадию аллергических реакций, а также уменьшает миграцию клеток воспаления; угнетает выделение медиаторов, участвующих в поздней стадии аллергической реакции. Устраняет кожную реакцию на введение гистамина, специфических аллергенов. На фоне курсового лечения толерантность к антигистаминному действию цетиризина не развивается. В рекомендуемой дозе цетиризин улучшает качество жизни пациентов, страдающих постоянным или сезонным аллергическим ринитом.
Для взрослых и детей 2 лет и старше:
— для облегчения назальных и глазных симптомов сезонного и круглогодичного аллергического ринита;
— для облегчения симптомов хронической идиопатической крапивницы.
Внутрь, независимо от приема пищи.
Препарат можно принимать в неразбавленном виде или разбавленный водой. При разбавлении водой, особенно при приеме детьми, следует учитывать, что объем воды для разбавления должен подбираться в зависимости от того, какое количество воды пациент в состоянии проглотить. Разбавленный раствор следует принимать немедленно.
Дети от 2 до 6 лет: 2,5 мг цетиризина (5 капель) 2 раза в сутки. В случае лечения симптомов сезонного ринита и конъюнктивита, продолжительность применения должна составлять не более 4 недель.
Дети от 6 до 12 лет: 5 мг цетиризина (10 капель) 2 раза в сутки. В случае лечения симптомов сезонного ринита и конъюнктивита, продолжительность применения должна составлять не более 4 недель.
Взрослые и дети старше 12 лет: 10 мг цетиризина (20 капель) 1 раз в сутки.
Пациенты пожилого возраста
Корректировка дозы не требуется при условии нормальной функции почек.
Пациенты с нарушением функции почек
Отсутствуют данные, подтверждающие эффективность/безопасность препарата у пациентов с нарушением функции почек. При отсутствии возможности применения альтернативного лечения, режим дозирования должен подбираться индивидуально в зависимости от состояния почечной функции. Коррекция дозы проводится в соответствии с указаниями приведенной ниже таблицы. Для использования данной таблицы необходимо определить клиренс креатинина (КК) в мл/мин. КК (мл/мин) можно рассчитать, исходя из установленной концентрации сывороточного креатинина (мг/дл), по следующей формуле:
.png)
КК для женщин можно рассчитать, умножив полученное значение на коэффициент 0,85.
Дозирование для пациентов с нарушением функции почек
| Стадия | КК (мл/мин) | Режим дозирования |
| Норма | ≥80 | 10 мг (20 капель)/сутки |
| Легкая | 50-79 | 10 мг (20 капель)/сутки |
| Средняя | 30-49 | 5 мг (10 капель)/сутки |
| Тяжелая | <30 | 5 мг (10 капель) один раз в два дня |
| Терминальная стадия — пациенты, находящиеся на диализе | <10 | Противопоказано |
Дети с нарушением функции почек
Дозу следует подбирать индивидуально, с учетом почечного клиренса, возраста и массы тела пациента.
Пациенты с нарушением функции печени
Пациентам, имеющим только нарушения функции печени, нет необходимости в коррекции дозы.
Пациенты с нарушениями функции печени и почек
Рекомендуется скорректировать дозу (см. раздел Пациенты с нарушением функции почек).
Продолжительность лечения препаратом необходимо устанавливать индивиду- ально.
Пропуск приема препарата
В случае пропуска приема препарата, примите пропущенную дозу как можно быстрее. Если уже приближается время очередного приема препарата, то примите одну дозу как обычно. Не принимайте двойную дозу препарата для компенсации пропущенной дозы.
Цетиризин в рекомендуемой дозе оказывает незначительное побочное действие на центральную нервную систему (ЦНС), проявляющееся в виде сонливости, усталости, головокружения и головной боли. В некоторых случаях, сообщалось о парадоксальном возбуждении ЦНС.
Частота развития нежелательных реакций приведена в следующей градации: нечасто — могут возникать менее чем у 1 человека из 100; редко — могут возникать менее чем у 1 человека из 1 000; очень редко — могут возникать менее чем у 1 человека из 10 000; частота неизвестна — исходя из имеющихся данных, частоту возникновения определить невозможно.
Нарушения со стороны крови и лимфатической системы:
очень редко: тромбоцитопения.
Нарушения со стороны иммунной системы: редко: гиперчувствительность; очень редко: анафилактический шок.
Нарушения метаболизма и питания: частота неизвестна: увеличение аппетита. Психические нарушения: нечасто: возбуждение; редко: агрессия, спутанность сознания, депрессия, галлюцинации, бессонница; очень редко: тики; частота неизвестна: кошмарные сновидения, суицидальные мысли.
Нарушения со стороны нервной системы: нечасто: парестезия; редко: судороги; очень редко: нарушения вкуса, обморок, тремор, дистония, дискинезия; частота неизвестна: амнезия, нарушение памяти, глухота.
Нарушения со стороны органа зрения: очень редко: нарушения аккомодации, окулогирный криз, нечеткость зрения; частота неизвестна: васкулит.
Нарушения со стороны органов слуха: частота неизвестна: головокружение. Нарушения со стороны сердца: редко: тахикардия.
Нарушения со стороны желудочно-кишечного тракта: нечасто: диарея.
Нарушения со стороны печени и желчевыводящих путей: редко: изменение показателей функции печени (повышение уровня трансаминаз, щелочной фосфатазы, ГГТ и билирубина).
Нарушения со стороны кожи и подкожных тканей’, нечасто: зуд, сыпь; редко: крапивница; очень редко: ангионевротический отек, стойкая лекарственная эритема; частота неизвестна: острый генерализованный экзантематозный пустулез.
Нарушения со стороны мышечной, скелетной и соединительной ткани: частота неизвестна: артралгии.
Нарушения со стороны почек и мочевыводящих путей: очень редко: дизурия, энурез; частота неизвестна: задержка мочеиспускания.
Общие нарушения и реакции в месте введения: нечасто: астения, недомогание; редко: отек.
Результаты инструментальных исследований: редко: увеличение веса.
В пострегистрационный период наблюдались следующие нежелательные эффекты: зуд и/или крапивница после прекращения терапии цетиризином.
Сообщение о нежелательных реакциях
Если у Вас возникают какие-либо нежелательные реакции, рекомендуется проконсультироваться с врачом. Данная рекомендация распространяется на любые возможные нежелательные реакции, в том числе на не перечисленные в листке- вкладыше. Вы также можете сообщить о нежелательных реакциях в информационную базу данных по нежелательным реакциям (действиям) на лекарственные препараты, включая сообщения о неэффективности лекарственных препаратов. Сообщая о нежелательных реакциях, Вы помогаете получить больше сведений о безопасности препарата.
— повышенная чувствительность к компонентам препарата, гидроксизину или любым другим производным пиперазина;
— тяжелая почечная недостаточность (клиренс креатинина менее 10 мл/мин).
Симптомы
Симптомы, наблюдающиеся при передозировке цетиризином, в основном связаны с действием на ЦНС и антихолинергическим действием. Возможны спутанность сознания, диарея, головокружение, усталость, головная боль, недомогание, расширение зрачков, зуд, беспокойство, седативный эффект, сонливость, заторможенность, тахикардия, тремор и задержка мочеиспускания (по крайней мере при приеме пятикратной дневной дозы цетиризина).
Лечение
Специфического антидота нет. Симптоматическая или поддерживающая терапия. Проводят промывание желудка, назначают активированный уголь при условии, что передозировка случилась недавно. Гемодиализ неэффективен.
При приеме в терапевтических дозах не наблюдалось клинически значимых взаимодействий с алкоголем (при уровне алкоголя в крови 0,5 г/л). Тем не менее, следует с осторожностью принимать лекарственный препарат совместно с алкоголем.
Рекомендуется соблюдать осторожность пациентам, предрасположенным к задержке мочеиспускания (например, пациенты с поражением спинного мозга или гиперплазией предстательной железы), ввиду того, что цетиризин может увеличивать риск задержки мочеиспускания.
Рекомендуется соблюдать осторожность при назначении препарата больным эпилепсией и пациентам с риском развития судорог.
Кожные тесты на аллергические реакции ингибируются при приеме антигистаминных средств, поэтому перед проведением тестирования необходим период в 3 дня без приема препарата.
После прекращения применения цетиризина может появиться зуд и/или крапивница, даже если эти симптомы отсутствовали в начале лечения. В некоторых случаях симптомы могут быть интенсивными и требовать возобновления приема цетиризина. Симптомы исчезают при возобновлении приема цетиризина.
Детская популяция
Не рекомендуется применение цетиризина у новорожденных и детей младше 2 лет.
Входящие в состав препарата метилпарагидроксибензоат и пропилпарагидроксибензоат могут вызывать аллергические реакции (возможно, отсроченные).
Лекарственное средство содержит 350 мг пропиленгликоля в 1 мл.
Беременность
Беременным женщинам препарат назначается с осторожностью.
Период кормления грудью
Цетиризин выделяется с грудным молоком, поэтому следует прекратить грудное вскармливание на период лечения.
Объективные измерения способности управлять транспортными средствами, латенции сна и производительности труда при работе на конвейере не продемонстрировали какие-либо клинически значимые эффекты при приеме рекомендуемой дозы 10 мг. Однако цетиризин может вызвать повышенную сонливость. Поэтому препарат может оказать влияние на способность управлять транспортными средствами или работать с механизмами.
Пациенты, намеревающиеся управлять транспортными средствами, участвовать в потенциально опасных видах деятельности или работать с механизмами, не должны превышать рекомендуемую дозу и должны учитывать собственный ответ на лекарственный препарат.
У чувствительных пациентов одновременное применение алкоголя или других депрессантов ЦНС может вызвать дополнительное снижение бдительности и ухудшение производительности труда.
Фармакокинетический и фармакодинамический профиль цетиризина не предполагает каких-либо взаимодействий с этим антигистаминным средством. Ни фармакодинамических, ни значительных фармакокинетических взаимодействий не было выявлено в исследованиях взаимодействия с другими лекарственными средствами, в частности, с псевдоэфедрином или теофиллином (400 мг/сут).
Совместное применение с азитромицином, циметидином, эритромицином, кетоконазолом или псевдоэфедрином не влияло на фармакокинетические параметры цетиризина. Не наблюдалось никаких фармакодинамических взаимодействий. Согласно исследованиям in vitro, цетиризин не влияет на связывание белка с варфа- рином.
Сопутствующее применение азитромицина, эритромицина, кетоконазола, теофиллина и псевдоэфедрина не выявило каких-либо существенных изменений в параметрах клинических лабораторных исследований, жизненно важных функций и ЭКГ.
После однократной дозы 10 мг цетиризин не оказывал существенного влияния на эффект алкоголя (0,8%о); для одного из 16 психометрических тестов было статистически значимое взаимодействие с диазепамом 5 мг. Одновременное применение цетиризина с алкоголем или другими веществами, угнетающими функции ЦНС, может привести к дополнительному снижению внимания.
Совместное применение 10 мг цетиризина ежедневно с глипизидом приводило к небольшому снижению уровня глюкозы. Этот эффект не имел клинического значения. Тем не менее, рекомендуется отдельный прием: глипизид утром, а цетиризин вечером.
Степень абсорбции цетиризина не уменьшается при одновременном приеме пищи, хотя скорость всасывания уменьшается на 1 час.
В исследовании с многократными дозами приема ритонавира (600 мг два раза в день) и цетиризина (10 мг/сутки) воздействие цетиризина было увеличено примерно на 40 %, тогда как воздействие ритонавира было слегка изменено (-11 %) при одновременном применении с цетиризином.
В защищенном от света месте при температуре не выше 25 °С.
Хранить в недоступном для детей месте.
2 года. Срок хранения после вскрытия упаковки — 6 недель.
Не использовать по истечении срока годности, указанного на упаковке.
По 20 мл во флаконы-капельницы из коричневого стекла, укупоренные полимерной пробкой капельницей и полимерной крышкой укупорочно-навинчиваемой с контролем первого вскрытия. Каждый флакон вместе с инструкцией по медицинскому применению помещают в пачку из картона.
Без рецепта.
Производитель:
ООО «АмантисМед»
Республика Беларусь, 223141, г. Логойск, ул. Минская 2и тел/факс: (+375 1774) 25 286
е-mail: office@amantismed.by
Тражента — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-001430-060217
Торговое наименование:
Тражента®
Международное непатентованное наименование:
линаглиптин
Лекарственная форма:
таблетки, покрытые пленочной оболочкой
Состав
1 таблетка, покрытая пленочной оболочкой, содержит:
действующее вещество: линаглиптин — 5 мг; вспомогательные вещества: маннитол — 130,9 мг, крахмал прежелатинизированный — 18 мг. крахмал кукурузный -18 мг, коповидон — 5,4 мг, магния стеарат — 2,7 мг; пленочная оболочка: Опадрай© розовый (02F34337) — 5 мг (гипромеллоза 2910 — 2,5 мг, титана диоксид (Е 171) — 1,25 мг, тальк — 0,875 мг, макрогол 6000 — 0,25 мг, краситель железа оксид красный (Е 172) — 0,125 мг).
Описание
Круглые двояковыпуклые со скошенными краями таблетки, покрытые пленочной оболочкой светло-красного цвета, с гравировкой символа компании на одной стороне и с гравировкой «D5» на другой стороне таблетки.
Фармакотерапевтическая группа
Гипогликемическое средство — дипептидилпептидазы — 4 ингибитор
Код ATX: А10ВН05
Фармакологические свойства
Фармакодинамика:
Линаглиптин является ингибитором фермента дипептидилпептидазы-4 (ДПП-4). который участвует в инактивации гормонов инкретинов — глюкагоноподобного пептида 1 типа (ГПП-1) и глюкозозависимого инсулинотропного полипептида (ГИП). Эти гормоны быстро разрушаются ферментом ДПП-4. Оба эти инкретина участвуют в поддержании концентрации глюкозы на физиологическом уровне. Базальные концентрации ГПП-1 и ГИП в течение суток низкие, они быстро повышаются в ответ на прием пищи. ГПП-1 и ГИП усиливают биосинтез инсулина и его секрецию бета-клетками поджелудочной железы при нормальной или повышенной концентрации глюкозы крови. Кроме того, ГПП-1 снижает секрецию глюкагона альфа-клетками поджелудочной железы, что приводит к уменьшению продукции глюкозы в печени. Линаглиптин активно связывается с ферментом ДПП-4 (связь обратимая), что вызывает устойчивое повышение концентрации инкретинов и длительное сохранение их активности. Препарат ТРАЖЕНТА* увеличивает глюкозозависимую секрецию инсулина и снижает секрецию глюкагона. что приводит к нормализации концентрации глюкозы в крови. Линаглиптин избирательно связывается с ферментом ДПП-4 и обладает в 10000 раз большей селективностью по отношению к ДПП-4 по сравнению с ферментами дипептидилпептидазы-8 или дипептидилпептидазы-9 in vitro.
В клинических исследованиях, где применялся линаглиптин в виде монотерапии. комбинированной терапии с метформином. комбинированной терапии с препаратами сульфонилмочевины. комбинированной терапии с инсулином, комбинированной терапии с метформином и препаратами сульфонилмочевины, комбинированной терапии с пиоглитазоном, комбинированной терапии с метформином и пиоглитазоном. комбинированной терапии с метформином в сравнении с глимепиридом было доказано статистически значимое снижение гликозилированного гемоглобина (HbAlc) и уменьшение концентрации ГПН (глюкоза плазмы натощак).
Применение линаглиптина у пациентов с тяжелой почечной недостаточностью, получавших адекватную базовую гипогликемическую терапию
В клинических исследованиях, где применялся линаглиптин в дополнение к базовой гипогликемической терапии (включающей инсулин, производные сульфонилмочевины. глиниды или пиоглитазон) было доказано статистически значимое снижение гликозилированного гемоглобина HbAlc (на 0,59% по сравнению с плацебо; исходное значение HbAlc составляло около 8,2 %).
Применение монотерапии линаглиптином и исходной комбинированной терапии линаглиптином и метформином у пациентов с недавно установленным диагнозом сахарного диабета 2 типа (с выраженной гипергликемией)
В ходе клинических исследований было доказано, что как монотерапия линаглиптином, так и комбинированная терапия линаглиптином и метформином приводили к статистически значимому снижению гликозилированного гемоглобина (HbAlc) на 2,0 % и 2,8 %, соответственно (исходное значение HbAlc составляло 9.9% и 9.8%, соответственно). Показатель разницы в методах лечения -0,8 % (95 % ДИ от -1,1 до — 0,5) продемонстрировал преимущества исходной комбинированной терапии линаглиптином и метформином над монотерапией линаглиптином (р<0,0001).
Фармакокинетика
Фармакокинетика линаглиптина была всесторонне изучена при применении у здоровых добровольцев и у пациентов с сахарным диабетом 2 типа. У здоровых добровольцев после приема линаглиптина в дозе 5 мг он быстро всасывался, максимальная концентрация линаглиптина в плазме (Сmax) достигалась через 1,5 часа.
Концентрация линаглиптина в плазме снижается трехфазно. Терминальный период полувыведения длительный, более 100 часов, что в основном обусловлено устойчивым связыванием линаглиптина с ферментом ДПП-4, однако, так как связь обратимая. накопления линаглиптина не происходит. Эффективный период полувыведения после многократного приема линаглиптина в дозе 5 мг составляет, примерно. 12 часов. В случае приема линаглиптина в дозе 5 мг 1 раз в день устойчивые концентрации линаглиптина в плазме достигаются после третьей дозы.
Фармакокинетика линаглиптина у здоровых добровольцев и у пациентов с сахарным диабетом 2 типа была, в целом, аналогичной.
Всасывание
Абсолютная биодоступность линаглиптина составляет, примерно. 30 %. Прием линаглиптина вместе с пищей, содержащей большое количество жиров, не оказывает клинически существенного влияния на фармакокинетику. В исследованиях in vitro показано, что линаглиптин является субстратом для Р-гликопротеина и изофермента CYP3A4. Ритонавир. как потенциальный ингибитор Р-гликопротеина и изофермента CYP3A4. может вдвое увеличивать значение AUC (площадь под кривой «концентрация -время»). Рифампицин, как потенциальный индуктор Р-гликопротеина и изофермента CYP3A4, может снижать значение AUC в период равновесного состояния фармакокинетики.
Распределение
Объем распределения после однократного внутривенного введения линаглиптина в дозе
5 мг здоровым добровольцам составляет, примерно, 1,110 литров, что указывает на
интенсивное распределение в тканях. Связывание линаглиптина с белками плазмы
зависит от его концентрации и составляет при концентрации 1 нмоль/л около 99 %, а при
концентрации более 30 нмоль/л — 75-89 %. что отражает насыщение связывания
линаглиптина с ДПП-4 по мере увеличения его концентрации. При высокой
концентрации, когда возникает полное насыщение ДПП-4, 70-80 % линаглиптина
связывается с другими белками плазмы (не с ДПП-4), а 30-20 % линаглиптина находится в плазме в несвязанном состоянии.
Метаболизм
Приблизительно 5 % линаглиптина выводится почками. Метаболизируется незначительная часть линаглиптина. Метаболизм играет второстепенную роль в выведении линаглиптина. Известен один основной метаболит линаглиптина, который не обладает фармакологической активностью.
Выведение
Преимущественный путь выведения — через кишечник. Через 4 дня после перорального применения меченого линаглиптина [14С] у здоровых добровольцев выводилось, примерно, 85 % дозы (через кишечник 80 % и почками 5 %) при клиренсе креатинина, примерно, 70 мл/мин.
Фармакокинетика у особых групп пациентов
Почечная недостаточность
У пациентов с легкой почечной недостаточностью (клиренс креатинина (КК) от 50 до <80 мл/мин.) воздействие линаглиптина в стационарную фазу было сопоставимо с воздействием препарата у здоровых испытуемых. При умеренной почечной недостаточности (КК от 30 до <50 мл/мин.) наблюдалось небольшое увеличение воздействия (примерно в 1,7 раза по сравнению со здоровыми испытуемыми).
Воздействие линаглиптина у пациентов с сахарным диабетом 2 типа и тяжелой почечной недостаточностью (КК <30 мл/мин.) было увеличено примерно в 1,4 раза по сравнению с пациентами с сахарным диабетом и нормальной функцией почек. Моделирование значений AUC линаглиптина у пациентов с терминальной стадией почечной недостаточности показало, что воздействие в этих случаях сравнимо с воздействием препарата у пациентов с умеренными или тяжелыми нарушениями функции почек. Не ожидается, что применение гемодиализа или перитонеального диализа позволит добиться выведения линаглиптина в терапевтически существенной степени. В связи с этим у пациентов с любой степенью почечной недостаточности изменений дозирования линаглиптина не требуется.
Печеночная недостаточность
У пациентов с легкой, умеренной и тяжелой печеночной недостаточностью (по классификации Чайлд-Пью) средние значения AUC и Сmax линаглиптина после его многократного применения в дозе 5 мг были сходны с соответствующими значениями у сопоставимых здоровых испытуемых. Изменений дозирования линаглиптина у пациентов с легкой, умеренной и тяжелой печеночной недостаточностью не требуется.
Индекс массы тела (ИМТ)
Изменений дозирования линаглиптина в зависимости от ИМТ не требуется.
Пол
Изменений дозирования линаглиптина в зависимости от пола не требуется.
Пациенты пожилого возраста
Изменений дозирования линаглиптина в зависимости от возраста не требуется, поскольку возраст не оказывал клинически значимого влияния на фармакокинетику линаглиптина по данным популяционного фармакокинетического анализа, проводившегося в клинических исследованиях. Как у пожилых пациентов (возраст 65-80 лет) так и у более молодых пациентов концентрации линаглиптина в плазме были сопоставимы.
Дети
Фармакокинетика линаглиптина у детей не изучалась.
Раса
Изменений дозирования линаглиптина в зависимости от расы не требуется. Раса не оказывала существенного влияния на концентрации линаглиптина в плазме по данным комбинированного анализа фармакокинетических данных, полученных у пациентов европеоидной расы, пациентов латиноамериканского происхождения, афро-американцев и пациентов азиатской расы. Кроме того, было установлено сходство фармакокинетических характеристик линаглиптина в специальных исследованиях, проводившихся у здоровых добровольцев европеоидной расы и жителей Японии и Китая, а также у пациентов афро-американцев с сахарным диабетом 2 типа.
Показания к применению
Сахарный диабет 2 типа:
- в качестве монотерапии — у пациентов с неадекватным контролем гликемии только на фоне диеты и физических упражнений, при непереносимости метформина или при противопоказании к его применению вследствие почечной недостаточности;
- в качестве двухкомпонентной комбинированной терапии с метформином, производными сульфонилмочевины или тиазолидиндионом в случае неэффективности диетотерапии, физических упражнений и монотерапии этими препаратами:
- в качестве трехкомпонентной комбинированной терапии с метформином и производными сульфонилмочевины в случае неэффективности диетотерапии, физических упражнений и комбинированной терапии этими препаратами;
- в качестве двухкомпонентной комбинированной терапии с инсулином или многокомпонентной терапии с инсулином и метформином и/или пиоглитазоном и/ или производными сульфонилмочевины в случае неэффективности диетотерапии, физических упражнений и комбинированной терапии этими препаратами.
Противопоказания
- Гиперчувствительность к любому компоненту препарата;
- Сахарный диабет 1 типа;
- Диабетический кетоацидоз;
- Беременность и период грудного вскармливания;
- Детский возраст до 18 лет.
С осторожностью
- Панкреатит в анамнезе;
- Пациенты старше 80 лет;
- Применение в комбинации с производными сульфонилмочевины и/или инсулином.
Применение при беременности и в период грудного вскармливания
Применение линаглиптина во время беременности противопоказано. Применение линаглиптина в период грудного вскармливания противопоказано. Данные, полученные в доклинических исследованиях у животных, свидетельствуют о проникновении линаглиптина и его метаболита в грудное молоко. Не исключается риск воздействия на новорожденных и детей при грудном вскармливании. При необходимости применения линаглиптина в период грудного вскармливания, кормление грудью необходимо прекратить.
Способ применения и дозы
Рекомендуемая доза составляет 5 мг (1 таблетка) 1 раз в день, внутрь. При назначении в дополнение к метформину, линаглиптин принимают одновременно с метформином, сохраняя ранее назначенную дозу метформина.
В случае применения линаглиптина в комбинации с производными сульфонилмочевины и/или инсулином возможно снижение дозы производных сульфонилмочевины или инсулина для уменьшения риска развития гипогликемии.
Препарат ТРАЖЕНТА* может приниматься независимо от приема пищи в любое время дня.
Действия при пропуске приема одной или нескольких доз лекарственного препарата:
При пропуске дозы, пациенту следует принять препарат, как только он об этом вспомнит. Не следует принимать двойную дозу в один день.
Особые группы пациентов
Для пациентов с почечной недостаточностью коррекция дозы линаглиптина не требуется. Для пациентов с нарушением функции печени коррекции дозы линаглиптина не требуется, однако клинический опыт у таких пациентов недостаточен.
Для пациентов пожилого возраста коррекции дозы не требуется. Однако, клинический опыт у пациентов старше 80 лет ограничен, поэтому лечение таких групп пациентов необходимо проводить с осторожностью.
Побочное действие
Частота побочных эффектов при приеме линаглиптина 5 мг была аналогичной частоте побочных эффектов при приеме плацебо.
Прекращение терапии из-за нежелательных явлений было выше в группе пациентов. получавших плацебо (4,3 %), чем в группе, получавших линаглиптин в дозе 5 мг (3,4 %). Нежелательные реакции, наблюдавшиеся у пациентов, получавших линаглиптин в качестве монотерапии и комбинированной терапии с другими гипогликемическими средствами в плацебо-контролируемых исследованиях, представлены ниже в Таблице (нежелательные реакции классифицировались по органам и системам и в соответствии с предпочитающимися в MedDRA терминами) с указанием их абсолютной частоты. Категории частоты определяются следующим образом: очень часто ( >1/10), часто (от ≥1/100 до <1/10), нечасто (от ≥1/1000 до <1/100), редко (от ≥1/10000 до <1/1000) или очень редко (<1/10000); выделяются также нежелательные реакции, частота которых неизвестна (не может быть оценена на основании имеющихся данных).
|
Классификация побочных эффектов по типу и частоте встречаемости |
||
|
Системно-органный класс |
Частота встречаемости |
Побочный эффект |
|
При монотерапии линаглиптином |
||
|
Нарушения со стороны иммунной системы |
Нечасто |
гиперчувствительность |
|
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения |
Нечасто |
кашель |
|
Нарушения со стороны желудочно-кишечного тракта |
Частота неизвестна |
панкреатит |
|
Инфекционные и паразитарные заболевания |
Нечасто |
назофарингит |
|
Лабораторные и инструментальные данные |
Редко |
повышение амилазы в плазме крови |
|
При применении линаглиптина с метформином |
||
|
Нарушения со стороны иммунной системы |
Нечасто |
гиперчувствительность |
|
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения |
Нечасто |
кашель |
|
Нарушения со стороны желудочно-кишечного тракта |
Частота неизвестна |
панкреатит |
|
Инфекционные и паразитарные заболевания |
Нечасто |
назофарингит |
|
Лабораторные и инструментальные данные |
Нечасто |
повышение амилазы в плазме крови |
|
При применении линаглиптина с производными сульфонилмочевины |
||
|
Нарушения со стороны иммунной системы |
Частота неизвестна |
гиперчувствительность |
|
Нарушения со стороны обмена веществ и питания |
Частота неизвестна |
гипертриглицеридемия |
|
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения |
Частота неизвестна |
кашель |
|
Нарушения со стороны желудочно-кишечного тракта |
Частота неизвестна |
панкреатит |
|
Инфекционные и паразитарные заболевания |
Частота неизвестна |
назофарингит |
|
Лабораторные и инструментальные данные |
Частота неизвестна |
повышение амилазы в плазме крови |
|
При применении линаглиптина с пиоглитазоном |
||
|
Нарушения со стороны иммунной системы |
Нечасто |
гиперчувствительность |
|
Нарушения со стороны обмена веществ и питания |
Частота неизвестна |
гиперлипидемия |
|
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения |
Частота неизвестна |
кашель |
|
Нарушения со стороны желудочно-кишечного тракта |
Частота неизвестна |
панкреатит |
|
Инфекционные и паразитарные заболевания |
Частота неизвестна |
назофарингит |
|
Лабораторные и инструментальные данные |
Часто |
увеличение массы тела |
|
Нечасто |
повышение амилазы в плазме крови |
|
|
При применении линаглиптина с инсулином |
||
|
Нарушения со стороны иммунной системы |
Нечасто |
гиперчувствительность |
|
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения |
Нечасто |
кашель |
|
Нарушения со стороны желудочно-кишечного тракта |
Нечасто |
панкреатит запор |
|
Инфекционные и паразитарные заболевания |
Нечасто |
назофарингит |
|
Лабораторные и инструментальные данные |
Частота неизвестна |
повышение амилазы в плазме крови |
|
При применении линаглиптина с метформином и производными сульфонилмочевины |
||
|
Нарушения со стороны иммунной системы |
Нечасто |
гиперчувствительность |
|
Нарушения со стороны обмена веществ и питания |
Очень часто |
гипогликемия |
|
Нарушения со стороны дыхательной системы. органов грудной клетки и средостения |
Час una неизвеа на |
кашель |
|
Нарушения со стороны желудочно-кишечного тракта |
Частота неизвестна |
панкреатит |
|
Инфекционные и паразитарные заболевания |
Частота неизвестна |
назофарингит |
|
Лабораторные и инструментальные данные |
Нечасто |
повышение амилазы в плазме крови |
|
Постмаркетинговыii опыт применения |
||
|
Нарушения со стороны иммунной системы |
Редко |
ангионевротический отек крапивница |
|
Нарушения со стороны желудочно-кишечного тракта |
Редко |
изъязвление слизистой оболочки полости рта |
|
Нарушения со стороны кожи и подкожных тканей |
Частота неизвестна |
буллезный пемфигоид |
|
Нечасто |
сыпь |
Профиль безопасности при применении комбинированной терапии линаглиптином, метформином и пиоглитазоном был сравним с профилем безопасности при применении монотерапии линаглиптином, комбинированной терапии линаглиптином и метформином и комбинированной терапии линаглиптином и пиоглитазоном.
Передозировка
Во время проведения контролируемых клинических исследований у здоровых добровольцев однократные дозы линаглиптина, достигавшие 600 мг (в 120 раз превышавшие рекомендуемую дозу), переносились хорошо. Опыта применения дозы, превышающей 600 мг, нет.
В случае передозировки рекомендуется использовать обычные меры поддерживающего характера, например, удаление неабсорбированного препарата из желудочно-кишечного тракта, осуществление клинического контроля и проведение симптоматического лечения.
Взаимодействие с другими лекарственными препаратами
Оценка лекарственных взаимодействий in vitro
Линаглиптин является слабым конкурентным ингибитором изофермента CYP3A4. Линаглиптин не ингибирует другие изоферменты CYP и не является их индуктором. Линаглиптин является субстратом для Р-гликопротеина (P-gp) и ингибирует в небольшой степени опосредованный Р-гликопротеином транспорт дигоксина.
Оценка лекарственных взаимодействий in vivo
Линаглиптин не оказывает клинически значимого влияния на фармакокинетику метформина, глибенкламида, симвастатина, пиоглитазона, варфарина, дигоксина и пероральных контрацептивных препаратов, что доказано в условиях in vivo, и основывается на низкой способности линаглиптина приводить к лекарственным взаимодействиям с субстратами для CYP3A4, CYP2C9, CYP2C8, Р-гликопротеином и транспортными молекулами органических катионов.
Метформин.
Совместное применение метформина (многократный ежедневный прием
дозы 850 мг 3 раза в день) и линаглиптина в дозе 10 мг 1 раз в день (выше
терапевтической дозы) у здоровых добровольцев не приводило к клинически значимым
изменениям фармакокинетики линаглиптина или метформина. Таким образом.
линаглиптин не является ингибитором транспорта органических катионов
Производные сульфонилмочевины.
Фармакокинетика линаглиптина (5 мг) не изменялась
при совместном применении с глибенкламидом (однократная доза глибурида 1,75 мг) и
многократного приема линаглиптина внутрь (по 5 мг). Однако отмечалось клинически незначительное снижение значений AUC и Сmax глибенкламида на 14 %. Поскольку глибенкламид метаболизируется в основном CYP2C9, эти данные также подтверждают вывод о том, что линаглиптин не является ингибитором CYP2C9. Не ожидается клинически существенных взаимодействий и с другими производными сульфонилмочевины (например, глипизидом и глимепиридом), которые как и глибенкламид, в основном метаболизируются с участием CYP2C9.
Тиазолидиндионы.
Совместное применение нескольких доз линаглиптина по 10 мг в день (выше терапевтической дозы) и пиоглитазона по 45 мг в день (многократный прием), который является субстратом для CYP2C8 и CYP3A4, не оказывало клинически значимого влияния на фармакокинетику линаглиптина или пиоглитазона, или активных метаболитов пиоглитазона. Это указывает на то, что линаглиптин in vivo не является ингибитором метаболизма, опосредуемого CYP2C8, и подтверждает заключение об отсутствии существенного ингибирующего влияния линаглиптина in vivo на CYP3A4.
Ритпонавир.
Совместное применение линаглиптина (однократная доза 5 мг внутрь) и ритонавира (многократный прием дозы 200 мг внутрь), активного ингибитора Р-гликопротеина (P-gp) и изофермента CYP3A4, увеличивало значения AUC и Стах линаглиптина, примерно, в 2 раза и в 3 раза, соответственно. Однако эти изменения фармакокинетики линаглиптина не считались значимыми. Поэтому клинически существенного взаимодействия с другими ингибиторами Р-гликопротеина и CYP3A4 не ожидается, и изменения дозы не требуется.
Рифампицин.
Многократное совместное применение линаглиптина и рифампицина. активного индуктора Р-гликопротеина и изофермента CYP3A4, приводило к снижению значений AUC и Сmax линаглиптина соответственно на 39.6 % и 43,8 %. и к снижению ингибирования базальной активности дипептидилпептидазы-4, примерно, на 30 %. Таким образом, ожидается, что клиническая эффективность линаглиптина, применяющегося в комбинации с активными индукторами Р-гликопротеина. будет сохраняться, хотя может проявляться не в полной мере.
Дигоксин.
Совместное многократное применение у здоровых добровольцев линаглиптина (5 мг в день) и дигоксина (0,25 мг в день) не оказывало влияния на фармакокинетику дигоксина. Таким образом, линаглиптин in vivo не является ингибитором транспорта. опосредуемого Р-гликопротеином.
Варфарин.
Линаглиптин. применявшийся многократно в дозе 5 мг в день, не изменял фармакокинетику варфарина, являющегося субстратом для CYP2C9, что свидетельствует об отсутствии у линаглиптина способности ингибировать CYP2C9.
Симвастатин.
Линаглиптин, применявшийся у здоровых добровольцев многократно в дозе 10 мг в день (выше терапевтической дозы), оказывал минимальное влияние на фармакокинетические показатели симвастатина, являющегося чувствительным субстратом для CYP3A4. После приема линаглиптина в дозе 10 мг совместно с симвастатином, применявшимся в суточной дозе 40 мг в течение 6 дней, величина AUC симвастатина повышалась на 34%, а величина Cmax _ на 10%. Таким образом, линаглиптин является слабым ингибитором метаболизма, опосредуемого CYP3A4.
Изменение дозы при одновременном приеме с препаратами, которые метаболизируются с участием CYP3A4, считается нецелесообразным.
Пероральные контрацептивные препараты.
Совместное применение линаглиптина в дозе 5 мг с левоноргестрелом или этинилэстрадиолом не изменяло фармакокинетику этих препаратов.
Особые указания
Препарат ТРАЖЕНТА противопоказан у пациентов с сахарным диабетом 1 типа или для лечения диабетического кетоацидоза.
Гипогликемия
Частота развития гипогликемии в случае применения линаглиптина в виде монотерапии была сопоставима с плацебо.
В клинических исследованиях сообщалось, что частота развития гипогликемии в случае применения линаглиптина в комбинации с препаратами, которые, как считается, не вызывают гипогликемию (метформин, производные тиазолидиндиона). была сходной с соответствующим эффектом плацебо.
Производные сульфонилмочевины и инсулин, как известно, вызывают гипогликемию. Поэтому в случае применения линаглиптина в комбинации с производными сульфонилмочевины и/или инсулином следует соблюдать осторожность. При необходимости возможно снижение дозы производных сульфонилмочевины или инсулина.
Применение линаглиптина не увеличивает риск развития сердечно — сосудистых заболеваний.
Линаглиптин в комбинированной терапии с другими пероральными гипогликемическими препаратами применялся у пациентов с тяжелой почечной недостаточностью.
Линаглиптин обеспечивал значительное снижение концентрации гликозилированного гемоглобина и концентрации глюкозы натощак.
Коррекции дозы при применении у пациентов с нарушениями функции почек, печени и у пожилых пациентов не требуется.
Применение линаглиптина у пациентов старше 70 лет
Применение линаглиптина приводило к значимому снижению гликозилированного гемоглобина (HbAlc) (на 0,64% по сравнению с плацебо; исходное значение HbAlc составляло около 7,8 %). Применение линаглиптина также приводило к существенному уменьшению концентрации глюкозы в плазме натощак (ГПН). Однако, клинический опыт у пациентов старше 80 лет ограничен, поэтому лечение таких групп пациентов необходимо проводить с осторожностью.
Кардиоваскулярный риск
Лечение линаглиптином не приводит к увеличению кардиоваскулярного риска. Первичная конечная точка (комбинация частоты возникновения или времени, проходившего до первого возникновения кардиоваскулярной смерти, нефатального инфаркта миокарда. нефатального инсульта или госпитализации в связи с нестабильной стенокардией) достигалась у пациентов, получавших линаглиптин. незначительно реже, чем в объединенной группе пациентов, получавших активные препараты сравнения и плацебо (относительный риск 0.78; 95 % доверительный интервал 0,55; 1,12).
Постмаркетинговый опыт применения:
У пациентов, принимающих линаглиптин, были зафиксированы случаи острого панкреатита. В случае подозрения на панкреатит прием препарата должен быть отменен.
Влияние на способность управлять транспортными средствами и механизмами
Исследований влияния препарата на способность управлять транспортными средствами и механизмами не проводилось. Однако в связи с возможным развитием гипогликемии (которая может проявляться в виде головной боли, сонливости, слабости. головокружения, спутанности сознания, раздражительности, голода, учащенного сердцебиения, потливости, панических атак), особенно при приеме линаглиптина в комбинации с производными сульфонилмочевины и/или инсулином, необходимо соблюдать осторожность при управлении транспортными средствами и механизмами.
Форма выпуска
Таблетки, покрытые пленочной оболочкой 5 мг.
По 7 таблеток в блистер из А1/А1. По 2, 4 или 8 блистеров с инструкцией по применению в картонную пачку.
По 10 таблеток в блистер. По 3 блистера с инструкцией по применению в картонную пачку.
Условия хранения
При температуре не выше 25 °С. Хранить в недоступном для детей месте.
Срок годности
3 года
Не следует принимать препарат по истечении срока годности.
Условия отпуска
По рецепту.
Наименование и адрес держателя регистрационного удостоверения
Берингер Ингельхайм Интернешнл ГмбХ, Германия Бингер Штрассе, 173, 55216 Ингельхайм-на-Рейне, Германия
Производство готовой лекарственной формы и первичная упаковка
Вест-Ворд Колумбус Инк.
1809 Уилсон Роуд, Колумбус, Огайо 43228, США
Вторичная упаковка и выпускающий контроль качества
Вест-Ворд Колумбус Инк.
1809 Уилсон Роуд, Колумбус, Огайо 43228, США
или
Берингер Ингельхайм Фарма ГмбХ и Ко.КГ
Бингер Штрассе 173, 55216 Ингельхайм-на-Рейне, Германия
Получить дополнительную информацию о препарате, а также направить свои претензии и информацию о нежелательных явлениях можно по следующему адресу в России
ООО «Берингер Ингельхайм»
125171. Москва, Ленинградское шоссе. 16А стр.3
Купить Тражента в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
С темой данной статьи напрямую или косвенно сталкивался каждый, независимо от роли в системе здравоохранения. Если рассматривать эту тему отдельно, то можно обнаружить в своих знаниях некоторые уязвимости и пробелы, которые периодически возникают и у меня. Поэтому через эту статью я хотел бы вместе с читателями вспомнить и ещё раз разложить основные моменты, а также, возможно, открыть что-то новое как для себя, так и для других.
Прежде всего — терминология. Только в конце обучения в университете я начал понимать как важны те слова, которые мы используем при общении. Медицина сейчас представляет собой в основном потоки информации, и очень многое передается с помощью слов. Если понимание терминов нарушено — нарушается и поток информации.
По определению ВОЗ неблагоприятная побочная реакция (adverse reaction) – это ответ на препарат, приносящий вред непреднамеренно и возникающий при использовании доз для профилактики, диагностики или терапии заболевания, а также для модификации физиологических функций.
Нежелательное событие (явление) – происходящее на фоне приема лекарственного средства, но связь не доказана.
Серьезная побочная реакция – приводит к госпитализации, продлению госпитализации или же переводу в отделение реанимации.
Существуют и другие, связанные с этой темой термины, но для понимания необходимы, прежде всего, эти три.
Итак, ниже показано переложение на временную линию.
Существуют разные подходы в классификации побочных реакций, но признанными в мире являются типы, предложенные ВОЗ, которые важны не столько названиями, сколько вытекающими из них характеристиками:
Самыми частыми по возникновению побочными реакциями являются кровотечения, на втором месте расположились нарушения кроветворения, на третьем — поражение печени.
Частота возникновений побочных реакций указывается в инструкции к препарату. Стоит обратить внимание, что слова, используемые для обозначения частоты, не случайны — за ними стоят конкретные цифры, определенные также ВОЗ:
Но что делать специалисту, который установил реакцию, ранее не зафиксированную? Врач обязан заполнить извещение о подозреваемой неблагоприятной побочной реакции (нпр) лекарственного средства.
Выдержка из письма Министерства Здравоохранения “О неблагоприятных побочных реакциях лекарственных средств”: “Для предоставления унифицированной информации о развитии побочной реакции на лекарственное средство разработана и утверждена Минздравом России специальная форма — извещение, которая, в случае развития такой реакции, должна быть заполнена и направлена в Научный центр экспертизы и государственного контроля лекарственных средств Минздрава России”.
Конечно, первым препятствием отправки такого извещения является страх специалиста перед вышестоящими органами. Только нужно отметить, что проверке подвергается не место оказания медицинской помощи, а производитель лекарственного средства.
Существуют также некоторые малоизвестные методологические и лабораторные инструменты для борьбы с побочными реакциями:
- Global trigger tool — использование «триггеров» для выявления неблагоприятных реакций.
- Омиксные технологии (геномика, метаболомика, транскриптомика) — благодаря новым технологиям (ПЦР, хроматография с масс-спектрометрией) появилась возможность индивидуального подхода к пациенту и предсказывания поведения лекарства в организме.
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
| Компоненты |
Таблетки 500 мг + 125 мг |
Таблетки 875 мг + 125 мг |
| Действующие вещества | ||
|
Амоксициллина тригидрат (соответствует амоксициллину) |
574,00 мг (500 мг) |
1004,50 мг (875 мг) |
|
Клавуланат калия (соответствует клавулановой кислоте) |
148,87 мг (125 мг) |
148,87 мг (125 мг) |
| Вспомогательные вещества | ||
| Ароматизатор тропическая смесь | 26,00 мг | 38,00 мг |
| Ароматизатор сладкий апельсин | 26,00 мг | 38,00 мг |
| Аспартам | 6,50 мг | 9,50 мг |
| Кремния диоксид коллоидный безводный | 13,00 мг | 18,00 мг |
| Краситель железа оксид желтый, Е 172 | 3,50 мг | 5,130 мг |
| Тальк | 13,00 мг | 18,00 мг |
| Касторовое масло гидрогенизированное | 26,00 мг | 36,00 мг |
| Целлюлоза микрокристаллическая кремнийсодержащая1 | до 1300,00 мг | до 1940,00 мг |
Продолговатые, восьмиугольные таблетки светло-желтого цвета, с вкраплениями коричневого цвета.
Антибиотик-пенициллин полусинтетический+бета-лактамаз ингибитор
ATX J01CR02 Амоксициллин в комбинации с ингибиторами ферментов
Фармакодинамика
Механизм действия
Амоксициллин — полусинтетический антибиотик широкого спектра действия, обладающий активностью против многих грамположительных и грамотрицательных микроорганизмов. В то же время, амоксициллин подвержен разрушению бета-лактамазами, и поэтому спектр активности амоксициллина не распространяется на микроорганизмы, которые продуцируют этот фермент.
Клавулановая кислота — ингибитор бета-лактамаз, структурно родственный пенициллинам, обладает способностью инактивировать широкий спектр бета-лактамаз, обнаруженных у микроорганизмов, устойчивых к пенициллинам и цефалоспоринам. Клавулановая кислота обладает достаточной эффективностью в отношении плазмидных бета-лактамаз, которые чаще всего обуславливают резистентность бактерий, и не эффективна в отношении хромосомных бета-лактамаз 1 типа, которые не ингибируются клавулановой кислотой.
Присутствие клавулановой кислоты в препарате защищает амоксициллин от разрушения ферментами — бета-лактамазами, что позволяет расширить антибактериальный спектр амоксициллина.
Ниже приведена активность комбинации амоксициллина с клавулановой кислотой in vitro.
Бактерии, обычно чувствительные к комбинации амоксициллина с клавулановой кислотой
Грамположительные аэробы:
Bacillus anthracis, Enterococcus faecalis, Listeria monocytogenes, Nocardia asteroides, Streptococcus pyogenes1,2, Streptococcus agalactiae1,2, Streptococcus spp. (другие бета-гемолитические стрептококки)1,2, Staphylococcus aureus (чувствительный к метициллину)1, Staphylococcus saprophyticus (чувствительный к метициллину), коагулазонегативные стафилококки (чувствительные к метициллину).
Грамположительные анаэробы:
Clostridium spp., Peptococcus niger, Peptostreptococcus та gnus, Peptostreptococcus micros, Peptostreptococcus spp.
Грамотрицательные аэробы:
Bordetella pertussis, Haemophilus influenzae1, Helicobacter pylori, Moraxella catarrhalis1, Neisseria gonorrhoeae, Pasteurella multocida, Vibrio cholerae.
Грамотрицательные анаэробы:
Bacteroides fragilis, Bacteroides spp., Capnocytophaga spp., Eikenella corrodens, Fusobacterium nucleatum, Fuso bacterium spp., Porphyromonas spp., Prevotella spp.
Прочие:
Borrelia burgdorferi, Leptospira icterohaemorrhagiae, Treponema pallidum.
Бактерии, для которых вероятна приобретенная резистентность к комбинации амоксициллина с клавулановой кислотой
Грамотрицательные аэробы:
Escherichia coli1, Klebsiella oxytoca, Klebsiella pneumoniae1, Klebsiella spp., Proteus mirabilis, Proteus vulgaris, Proteus spp., Salmonella spp., Shigella spp.
Грамположительные аэробы:
Corynebacterium spp., Enterococcus faecium, Streptococcus pneumoniae1,2, стрептококки группы Viridans2.
Бактерии, обладающие природной устойчивостью к комбинации амоксициллина с клавулановой кислотой
Грамотрицательные аэробы:
Acinetobacter spp., Citrobacter freundii, Enterobacter spp., Hafnia alvei, Legionella pneumophila, Morganella morganii, Providencia spp., Pseudomonas spp., Serratia spp., Stenotrophomonas maltophilia, Yersinia enterocolitica.
Прочие:
Chlamydophila pneumoniae, Chlamydophila psittaci, Chlamydia spp., Coxiella burnetii, Mycoplasma spp.
1для данных видов микроорганизмов клиническая эффективность комбинации амоксициллина с клавулановой кислотой была продемонстрирована в клинических исследованиях.
2штаммы этих видов бактерий не продуцируют β-лактамазы.
Чувствительность при монотерапии амоксициллином позволяет предполагать аналогичную чувствительность к комбинации амоксициллина с клавулановой кислотой.
Фармакокинетика
Всасывание
Амоксициллин и клавулановая полностью диссоциируют в водном растворе при физиологических значениях pH. Оба активных компонента препарата, амоксициллин и клавулановая кислота, быстро и хорошо всасываются из желудочно-кишечного тракта (ЖКТ) после перорального приема. Абсорбция действующих веществ оптимальна в начале приема пищи. Биодоступпость амоксициллина и клавулановой кислоты при приеме внутрь высокая.
После однократного приема препарата в дозе 500 мг амоксициллина /125 мг клавулановой кислоты максимальная концентрация амоксициллина в плазме крови создается через 1,5 ч (1,0-2,5 ч), и составляет 7,19±2,26 мкг/мл (Сmах), клавулановой кислоты — через 1,5 ч (1,0-2,0 ч), составляя 2,4±0,83 мкг/мл.
ПФК (показатель «площадь под фармакокинетической кривой») амоксициллина и клавулановой кислоты составляет 53,5±8,87 мкг*ч/л и 15,72±3,86 мкг*ч/л, соответственно.
Плазменные концентрации амоксициллина и клавулановой кислоты, достигаемые при применении амоксициллин/клавуланата, схожи с таковыми при пероральном приеме эквивалентных доз амоксициллина и клавулановой кислоты по отдельности.
Распределение
Приблизительно около 18% амоксициллина и 25% клавулановой кислоты связываются с белками плазмы крови. Кажущийся объем распределения составляет 0,3-0,4 л/кг для амоксициллина и около 0,2 л/кг для клавулановой кислоты. Амоксициллин плохо распределяется в спинномозговую жидкость.
В исследованиях на животных кумуляции компонентов препарата в тканях организма не выявлено.
Как и большинство пенициллинов, амоксициллин проникает в грудное молоко. Клавулановая кислота также обнаруживается в грудном молоке в следовых концентрациях.
Амоксициллин и клавулановая кислота проникают через плацентарный барьер.
Метаболизм
10-25% от начальной дозы амоксициллина выводится почками в виде неактивного метаболита (пенициллоевой кислоты).
Клавулановая кислота подвергается интенсивному метаболизму и выводится почками, кишечником, а также с выдыхаемым воздухом, в виде диоксида углерода.
Выведение
После однократного приема препарата в дозе 500 мг/125 мг период полувыведения амоксициллина составляет 1,15±0,20 ч, клавулановой кислоты — 0,98±0,12 ч, общий клиренс — около 25 л/ч.
Приблизительно 60-70% амоксициллина и около 40-65% клавулановой кислоты выводится почками в неизмененном виде в течение первых 6 часов после приема 1 таблетки препарата 250/125 мг или 500/125 мг. Наибольшее количество клавулановой кислоты экскретируется в течение первых 2 часов после приема. В различных исследованиях было показано, что в течение 24 часов через почки выводится до 50-85% амоксициллина и до 27-60% клавулановой кислоты.
Одновременный прием пробенецида задерживает выведение амоксициллина, но не влияет на экскрецию почками клавулановой кислоты (см. раздел «Взаимодействие с другими лекарственными препаратами»).
Фармакокинетика в особых случаях
Возрастные особенности
Период полувыведения амоксициллина у детей 3 месяцев — 2 лет не отличается от такового у детей старшего возраста и взрослых. Детям первой недели жизни (в том числе недоношенным) не следует назначать препарат более 2 раз в день из-за незрелости почечного пути элиминации. Из-за возможного снижения функции почек подбор дозы препарата для пожилых пациентов следует производить с осторожностью. Может потребоваться контроль функции почек.
Половые особенности
При пероральном приеме амоксициллин/клавулановой кислоты здоровыми мужчинами и женщинами не установлено значимого влияния пола пациента на фармакокинетику активных компонентов препарата.
Нарушение функции почек
Суммарный клиренс амоксициллин/клавулановой кислоты уменьшается пропорционально снижению почечной функции. Особенно заметно нарушается клиренс амоксициллина, поскольку почками экскретируется большая его часть. Таким образом, при нарушении функции почек следует корректировать дозу препарата во избежание избыточной концентрации амоксициллина и для поддержания необходимого уровня клавулановой кислоты.
Нарушение функции печени
У пациентов с нарушением функции печени препарат следует назначать с осторожностью. Необходимо регулярно контролировать функцию печени.
Комбинация амоксициллина с клавулановой кислотой показана для лечения бактериальных инфекций следующих локализаций, вызванных чувствительными к комбинации амоксициллина с клавулановой кислотой микроорганизмами:
— инфекции верхних дыхательных путей (включая инфекции ЛОР-органов), например, рецидивирующий тонзиллит, синусит, средний отит, обычно вызываемые Streptococcus pneumoniae, Haemophilus influenzae#, Moraxella catarrhalis и Streptococcus pyogenes.
— инфекции нижних отделов дыхательных путей, например, обострения хронического бронхита, долевая пневмония и бронхопневмония, обычно вызываемые Streptococcus pneumoniae, Haemophilus influenza и Moraxella catarrhalis#.
— инфекции мочеполового тракта, например, цистит, уретрит, пиелонефрит, инфекции женских половых органов, обычно вызываемые видами семейства Enterobacteriaceae (преимущественно Escherichia coli#), Staphylococcus saprophyticus и видами рода Enterococcus, а также гонорея, вызываемая Neisseria gonorrhoeae#.
— инфекции кожи и мягких тканей, обычно вызываемые Staphylococcus aureus#, Streptococcus pyogenes и видами рода Bacteroides#.
— инфекции костей и суставов, например, остеомиелит, обычно вызываемый Staphylococcus aureus#, при необходимости возможно проведение длительной терапии.
— одонтогенные инфекции, например, периодонтит, одонтогенный верхнечелюстной синусит, тяжелые дентальные абсцессы с распространяющимся целлюлитом.
— другие смешанные инфекции (например, септический аборт, послеродовой сепсис, интраабдоминальный сепсис) в рамках ступенчатой терапии.
#Отдельные представители указанного рода микроорганизмов продуцируют бета-лактамазу, что делает их нечувствительными к амоксициллину (см. также раздел «Фармакологические свойства»).
Инфекции, вызванные чувствительными к амоксициллину микроорганизмами, можно лечить препаратом Амоксиклав® Квиктаб, поскольку амоксициллин является одним из его активных ингредиентов. Амоксиклав® Квиктаб также показан для лечения смешанных инфекций, обусловленных микроорганизмами, чувствительными к амоксициллину, а также микроорганизмами, продуцирующими бета-лактамазу, чувствительными к комбинации амоксициллина с клавулановой кислотой.
Чувствительность бактерий к комбинации амоксициллина с клавулановой кислотой варьирует в зависимости от региона и с течением времени. Там, где это возможно, должны быть приняты во внимание локальные данные по чувствительности. В случае необходимости следует проводить сбор микробиологических образцов и анализ на бактериологическую чувствительность.
— Повышенная чувствительность к амоксициллину, клавулановой кислоте, другим пенициллинам или другим вспомогательным веществам препарата;
— тяжелые реакции гиперчувствительности (например, анафилактические реакции) в анамнезе к другим бета-лактамным антибиотикам (цефалоспорины, карбапенемы или монобактамы);
— холестатическая желтуха и/или другие нарушения функции печени, вызванные приемом амоксициллина/клавулановой кислоты, в анамнезе;
— дети до 12 лет или с массой тела меньше 40 кг;
— фенилкетонурия;
— почечная недостаточность (КК ≤30 мл/мин) (для таблеток диспергируемых 875 мг+125 мг).
С осторожностью: Тяжелая печеночная недостаточность; заболевания желудочно-кишечного тракта (в т.ч. колит, связанный с применением пенициллинов в анамнезе); хроническая почечная недостаточность; беременность; период грудного вскармливания; одновременное применение с антикоагулянтами.
Исследования на животных не выявили данных о вреде приема препарата Амоксиклав® Квиктаб в период беременности и его воздействии на эмбриональное развитие плода.
В одном исследовании у женщин с преждевременным разрывом околоплодных оболочек было установлено, что профилактическая терапия амоксициллином/клавулановой кислотой может быть связана с повышением риска развития некротизирующего энтероколита у новорожденных. Также есть сведения о развитии у новорожденных диареи и кандидоза слизистых оболочек полости рта.
При беременности и в период лактации препарат Амоксиклав® Квиктаб применяют только в том случае, если предполагаемая польза для матери превышает потенциальный риск для плода и ребенка.
Амоксициллин и клавулановая кислота в небольших количествах проникают в грудное молоко, поэтому прием препарата в период грудного вскармливания должен быть продолжен только при наличии четких показаний.
У младенцев, получающих грудное вскармливание, возможно развитие сенсибилизации, диареи, кандидоза слизистых оболочек полости рта. В подобных случаях грудное вскармливание следует прекратить.
Внутрь.
Режим дозирования устанавливается индивидуально в зависимости от возраста, массы тела, функции почек пациента и степени тяжести инфекции.
Таблетки необходимо растворить в половине стакана воды (минимум 30 мл) и тщательно перемешать, затем выпить, или подержать таблетки во рту до полного растворения, после чего проглотить. С целью снижения риска развития побочных эффектов со стороны ЖКТ следует принимать препарат в начале еды.
Диспергируемые таблетки препарата Амоксиклав® Квиктаб 500 мг/125 мг:
Взрослые и дети старше 12 лет с массой тела ≥40 кг:
Для лечения инфекций легкой и средней степени тяжести — одна таблетка (500 мг/125 мг) каждые 12 ч (2 раза в день).
Для лечения тяжелых инфекций и инфекций органов дыхания — одна таблетка (500 мг/125 мг) каждые 8 ч (3 раза в день).
Максимальная суточная доза препарата Амоксиклав® Квиктаб составляет 1500 мг амоксициллина/375 мг клавулановой.
Пациенты с нарушением функции почек
У пациентов с клиренсом креатинина (КК) выше 30 мл/мин отсутствует необходимость в коррекции дозы.
Взрослые и дети старше 12 лет с массой тела ≥ 40 кг (указанный режим дозирования применяется при инфекциях среднего и тяжелого течения):
| КК: 10-30 мл/мин | 500 мг/125 мг 2 раза в день (при среднем и тяжелом течении инфекции) |
| КК < 10 мл/мин | 500 мг/125 мг 1 раз в день (при среднем и тяжелом течении инфекции) |
| Гемодиализ | 500 мг/125 мг каждые 24 ч, плюс 500 мг/125 мг во время сеанса диализа, с повторным применением в конце сеанса диализа (так как концентрации амоксициллина и клавулановой кислоты в плазме крови снижаются) |
Диспергируемые таблетки препарата Амоксиклав® Квиктаб 875 мг/125 мг:
Взрослые и дети старше 12 лет с массой тела ≥ 40 кг:
При тяжелых инфекциях и инфекциях органов дыхания — одна таблетка (875 мг/125 мг) каждые 12 часов (2 раза в день).
Суточная доза препарата Амоксиклав®Квиктаб при применении 2 раза в день составляет 1750 мг амоксициллина/250 мг клавулановой кислоты.
Пациенты с нарушением функции почек
У пациентов с клиренсом креатинина (КК) более 30 мл/мин отсутствует необходимость в коррекции дозы.
Пациентам с КК менее 30 мл/мин использование диспергируемых таблеток препарата Амоксиклав® Квиктаб, 875 мг/125 мг противопоказано.
Таким пациентам следует принимать препарат в дозировке 500 мг/125 мг после соответствующей уровню КК коррекции дозы.
Пациенты с нарушением функции печени
При приеме препарата Амоксиклав® Квиктаб следует соблюдать осторожность. Необходимо проводить регулярный контроль функции печени. В случае начала лечения с парентерального введения препарата, терапию возможно продолжить приемом таблеток препарата Амоксиклав® Квиктаб.
Продолжительность курса лечения определяется лечащим врачом!
Минимальный курс антибактериальной терапии составляет 5 дней. Лечение не должно продолжаться более 14 дней без пересмотра клинической ситуации.
Нежелательные реакции, представленные ниже, перечислены в соответствии с поражением органов и систем органов и частотой встречаемости.
Частота встречаемости определяется следующим образом: очень часто (≥1/10), часто (≥1/100, <1/10), нечасто (≥1/1000, <1/100), редко (≥1/10000, <1/1000), очень редко (< 1/10000), частота неизвестна (не может быть установлена на основании имеющихся данных).
Категории частоты были сформированы на основании клинических исследований препарата и пострегистрационного наблюдения.
Частота встречаемости нежелательных реакций
Инфекционные и паразитарные заболевания
Часто: кандидоз кожи и слизистых оболочек.
Частота неизвестна: избыточный рост чувствительных микроорганизмов.
Нарушения со стороны крови и лимфатической системы
Редко: обратимая лейкопения (включая нейтропению), обратимая тромбоцитопения.
Частота неизвестна: обратимый агранулоцитоз и обратимая гемолитическая анемия, удлинение времени кровотечения и протромбинового времени.
Нарушения со стороны иммунной системы
Частота неизвестна: ангионевротический отек, анафилактические реакции, синдром, сходный с сывороточной болезнью, аллергический васкулит, острый коронарный синдром, ассоциированный с гиперчувствительностью (синдром Коуниса).
Нарушения со стороны нервной системы
Нечасто: головокружение, головная боль.
Частота неизвестна: обратимая гиперактивность, асептический менингит, судороги. Судороги могут наблюдаться у пациентов с нарушениями функции почек, а также у тех, кто получает высокие дозы препарата (см. разделы «Способ применения и дозы» — Пациенты с нарушением функции почек, «Передозировка»).
Нарушения со стороны желудочно-кишечного тракта
Взрослые:
Очень часто: диарея.
Часто: тошнота, рвота.
Дети:
Часто: диарея, тошнота, рвота.
Вся популяция:
Тошнота наиболее часто была связана с использованием высоких доз препарата. Если после начала приема препарата наблюдаются нежелательные реакции со стороны ЖКТ, они могут быть устранены, если принимать препарат в начале приема пищи.
Нечасто: нарушение пищеварения.
Частота неизвестна: антибиотикоассоциированный колит (включая псевдомембранозный колит и геморрагический колит) (см. раздел «Особые указания»), черный «волосатый» язык.
Нарушения со стороны печени и желчевыводящих путей
Нечасто: умеренное повышение активности аспартатаминотрансферазы и/или аланинаминотрансферазы (ACT и/или АЛТ). Данная реакция наблюдается у пациентов, получающих терапию бета-лактамными антибиотиками, однако клиническая значимость ее неизвестна.
Частота неизвестна: гепатит и холестатическая желтуха. Данные реакции наблюдаются у пациентов, получающих терапию антибиотиками пенициллинового ряда и цефалоспоринами.
Нежелательные реакции со стороны печени наблюдались, главным образом, у мужчин и пациентов пожилого возраста и могут быть связаны с длительной терапией. Данные нежелательные реакции очень редко наблюдаются у детей. Перечисленные признаки и симптомы обычно встречаются в процессе или сразу по окончании терапии, однако в отдельных случаях могут не проявляться в течение нескольких недель после завершения терапии. Нежелательные реакции, как правило, обратимы. Нежелательные реакции со стороны печени могут быть тяжелыми, в исключительно редких случаях были сообщения о летальных исходах. Почти во всех случаях это были лица с серьезной сопутствующей патологией или пациенты, получающие одновременно потенциально гепатотоксичные препараты.
Нарушения со стороны кожи и подкожных тканей
Нечасто: сыпь, зуд, крапивница.
Редко: многоформная экссудативная эритема.
Частота неизвестна: синдром Стивенса-Джонсона, токсический эпидермальный некролиз, буллезный эксфолиативный дерматит, острый генерализованный экзантематозный пустулез (AGEP) и лекарственная сыпь с эозинофилией и системными симптомами (DRESS).
В случае возникновения кожных аллергических реакций лечение препаратом Амоксиклав® Квиктаб необходимо прекратить.
Нарушения со стороны почек и мочевыводящих путей
Частота неизвестна: интерстициальный нефрит, кристаллурия (см. раздел «Передозировка»).
Сообщений о летальном исходе или возникновении угрожающих жизни побочных эффектов вследствие передозировки препарата Амоксиклав® Квиктаб нет.
Симптомы передозировки включают расстройства со стороны ЖКТ (боль в области живота, диарея, рвота) и нарушения водно-электролитного баланса. Зарегистрированы сообщения о кристаллурии, вызванной приемом амоксициллина, которая, в некоторых случаях, приводила к развитию почечной недостаточности.
Возможно развитие судорог у пациентов с почечной недостаточностью или у пациентов, получающих высокие дозы препарата.
При передозировке пациент должен находиться под наблюдением врача, лечение симптоматическое.
При передозировке препарата рекомендовано промывание желудка и прием адсорбентов (активированный уголь).
Гемодиализ эффективен.
Одновременное применение препарата Амоксиклав® Квиктаб и пробенецида не рекомендовано. Пробенецид снижает канальцевую секрецию амоксициллина, и поэтому одновременное применение препарата Амоксиклав® Квиктаб и пробенецида может приводить к повышению и персистенции в крови концентрации амоксициллина, но не клавулановой кислоты.
Одновременное использование аллопуринола и амоксициллина может повышать риск возникновения кожных аллергических реакций. В настоящее время в литературе нет данных об одновременном применении комбинации амоксициллина с клавулановой кислотой и аллопуринола.
Пенициллины способны замедлять выведение из организма метотрексата за счет ингибирования его канальцевой секреции, поэтому, одновременное применение препарата Амоксиклав® Квиктаб и метотрексата может увеличить токсичность метотрексата.
Как и другие антибактериальные препараты, препарат Амоксиклав® Квиктаб может оказывать влияние на кишечную микрофлору, приводя к снижению всасывания эстрогенов их ЖКТ и снижению эффективности комбинированных перроральных контрацептивов.
В литературе описываются редкие случаи увеличения международного нормализованного отношения (МНО) у пациентов при совместном применении аценокумарола или варфарина и амоксициллина. При необходимости одновременного назначения препарата Амоксиклав® Квиктаб с антикоагулянтами протромбиновое время или МНО должны тщательно контролироваться при назначении или отмене препарата Амоксиклав® Квиктаб, может потребоваться коррекция дозы антикоагулянтов для приема внутрь.
У пациентов, получавших микофенолата мофетил, после начала применения комбинации амоксициллина с клавулановой кислотой наблюдалось снижение концентрации активного метаболита — микофеноловой кислоты до приема очередной дозы препарата приблизительно на 50%. Изменения данной концентрации не могут точно отображать общие изменения экспозиции микофеноловой кислоты.
Перед началом лечения препаратом Амоксиклав® Квиктаб необходимо собрать подробный анамнез, касающийся предшествующих реакций гиперчувствительности на пснициллины, цефалоспорины или другие вещества, вызывающие аллергическую реакцию у пациента. Описаны серьезные, а иногда и летальные, реакции гиперчувствительности (включая анафилактические и тяжелые кожные нежелательные реакции) на пенициллины. Риск возникновения таких реакций наиболее высок у пациентов, имеющих в анамнезе реакции гиперчувствительности на пенициллины.
В случае возникновения аллергической реакции необходимо прекратить лечение препаратом Амоксиклав® Квиктаб и начать соответствующую альтернативную терапию.
В случае если доказано, что инфекция вызвана чувствительными к амоксициллину микроорганизмами, следует рассмотреть возможность замены комбинации амоксициллин/клавулановая кислота на амоксициллин в соответствии с официальными клиническими рекомендациями.
Комбинация амоксициллин/клавулановая кислота не подходит для применения в случаях, когда высок риск того, что предполагаемые патогенные микроорганизмы обладают пониженной чувствительностью или резистентностью к бета-лактамным препаратам, которая, не обусловлена бета-лактамазами, восприимчивыми к ингибированию клавулановой кислотой.
Амоксициллин/клавулановую кислоту не следует применять для терапии инфекций, вызванных резистентными к пенициллину штаммами S. pneumoniae.
Острый коронарный синдром, ассоциированный с гиперчувствительностью (синдром Коуниса)
В редких случаях сообщалось о реакциях гиперчувствительности во время лечения амоксициллином (острый коронарный синдром, ассоциированный с гиперчувствительностью), в этих случаях необходимо назначать соответствующее лечение.
У пациентов с нарушением функции почек, а также при приеме высоких доз препарата могут наблюдаться судороги (см. раздел «Побочные действия»).
В случае подозрения на инфекционный мононуклеоз не следует применять препарат Амоксиклав® Квиктаб, поскольку у пациентов с этим заболеванием амоксициллин может вызывать экзантему (кореподобную сыпь).
Одновременное применение аллопуринола во время лечения амоксициллином может повышать вероятность возникновения кожных аллергических реакций.
Длительное лечение препаратом Амоксиклав® Квиктаб может приводить к чрезмерному росту нечувствительных микроорганизмов.
Возникновение в начале лечения генерализованной эритемы с лихорадкой, сопровождаемой образованием пустул, может быть симптомом острого генерализованного экзантематозного пустулеза (ОГЭП). Такая реакция требует отмены препарата, содержащего амоксициллин/клавулановую кислоту, и является противопоказанием к последующему применению препаратов амоксициллина.
Препараты, содержащие амоксициллин/клавулановую кислоту, следует применять с осторожностью у пациентов с нарушениями функции печени. Нежелательные явления со стороны печени наблюдались, главным образом, у мужчин, и пациентов пожилого возраста и могут быть связаны с длительной терапией. Данные нежелательные явления очень редко наблюдаются у детей. Во всех популяциях перечисленные признаки и симптомы обычно встречаются в процессе или вскоре после окончания терапии, однако в некоторых случаях могут проявляться и через несколько недель после завершения терапии. Они, как правило, обратимы. Нежелательные явления со стороны печени могут быть тяжелыми, в исключительно редких случаях сообщалось о смертельных исходах. Почти во всех случаях это были пациенты с серьезными сопутствующими заболеваниями или пациенты, одновременно получающими препараты, потенциально влияющие на печень.
Описаны случаи возникновения псевдомембранозного колита при приеме антибиотиков, степень тяжести которого может варьироваться от легкой до угрожающей жизни. Поэтому важно учитывать возможность развития псевдомембранозного колита у пациентов с диареей во время или после применения антибиотиков. При возникновении антибиотик-ассоциированного колита следует немедленно прекратить лечение комбиницией амоксициллин/клавулановая кислота, обратиться к врачу и начать соответствующее лечение. Препараты, тормозящие перистальтику кишечника, противопоказаны в данной ситуации.
Во время длительной терапии препаратом Амоксиклав® Квиктаб рекомендуется периодически оценивать функцию почек, печени и кроветворения.
У пациентов, получавших комбинацию амоксициллина с клавулановой кислотой, в редких случаях сообщалось об удлинении протромбинового времени (повышении МНО). При одновременном применении непрямых (пероральных) антикоагулянтов с комбинацией амоксициллина с клавулановой кислотой необходим контроль соответствующих показателей.
Для поддержания необходимого эффекта пероральных антикоагулянтов может потребоваться коррекция их дозы.
У пациентов с нарушением функции почек дозу препарата Амоксиклав® Квиктаб следует снижать соответственно степени нарушения (см. раздел «Способ применения и дозы» — «Пациенты с нарушением функции почек»).
У пациентов со сниженным диурезом очень редко возникает кристаллурия, преимущественно при парентеральной терапии. Во время введения высоких доз амоксициллина рекомендуется принимать достаточное количество жидкости и поддерживать адекватный диурез для уменьшения вероятности образования кристаллов амоксициллина (см. раздел «Передозировка»). У пациентов с катетерами мочевого пузыря следует регулярно проверять их проходимость.
Прием препарата Амоксиклав® Квиктаб внутрь приводит к высокому содержанию амоксициллина в моче, что может приводить к ложноположительным результатам при определении глюкозы в моче (например, проба Бенедикта, проба Фелинга). В этом случае рекомендуется применять глюкозоксидантный (ферментативный) метод определения концентрации глюкозы в моче.
Клавулановая кислота может вызывать неспецифическое связывание иммуноглобулинов класса G и альбумина с мембранами эритроцитов, что приводит к ложноположительным результатам пробы Кумбса.
Сообщалось о положительных результатах теста Плателли Aspergillus с использованием тест- системы для иммуноферментного анализа (ИФА) компании Bio-Rad Laboratories у пациентов, получавших комбинацию амоксициллин/клавулановая кислота, у которых впоследствии не была обнаружена Aspergillus инфекция. При проведении теста Плателли Aspergillus ИФА сообщалось о перекрестных реакциях с полисахаридами и полифуранозами, не характерными для Aspergillus. В связи с этим положительные результаты теста Плателли Aspergillus ИФА у пациентов, получавших комбинацию амоксициллин/клавулановая кислота, следует интерпретировать с осторожностью и подтверждать другими методами диагностики.
В одной диспергируемой таблетке Амоксиклав® Квиктаб 500 мг/125 мг содержится 0,63 ммоль (24,53 мг) калия, в 875 мг/125 мг содержится 0,63 ммоль (24,53 мг) калия. Прием калия более 1 ммоль в сутки требует особого внимания у пациентов со сниженной функцией почек и находящихся на контролируемой калиевой диете.
Специальные меры предосторожности при уничтожении неиспользованного лекарственного препарата
Нет необходимости в специальных мерах предосторожности при уничтожении неиспользованного препарата Амоксиклав®Квиктаб.
Данных об отрицательном влиянии препарата Амоксиклав® Квиктаб в рекомендуемых дозах на способность к управлению автомобилем или работу с механизмами нет. Однако из-за возможности развития побочных эффектов со стороны центральной нервной системы, таких, как головокружение, головная боль, судороги, во время лечения следует соблюдать осторожность при управлении автомобилем и занятиях другими видами деятельности, требующими концентрации внимания и быстроты психомоторных реакций. При появлении описанных нежелательных явлений следует воздержаться от выполнения указанных видов деятельности.
Таблетки диспергируемые, 500 мг+125 мг и 875 мг+125 мг.
Первичная упаковка
По 2 таблетки в блистер из алюминия/алюминия.
Вторичная упаковка
По 5 или 7 блистеров вместе с инструкцией по медицинскому применению в пачку картонную.
Хранить в оригинальной упаковке (блистер в пачке), при температуре не выше 25 °С.
Хранить в недоступном для детей месте.
3 года.
Не использовать после истечения срока годности.
По рецепту
Регистрационный номер:ЛСР-005243/08
Дата регистрации:2008-07-04
Дата переоформления:2020-05-19
Владелец регистрационного удостоверения
САНДОЗ Д Д
Словения
Производитель:
ЛЕК Д Д
Словения
Представительство
САНДОЗ
Швейцария
Дата обновления информации: 2021-01-02
Лучший ответ по мнению автора
|
|||||||||||||||
Посмотреть всех экспертов из раздела Медицина
Читаю описания лекарственных препаратов и постоянно поражаюсь. Откуда? Или я чего не понимаю, или фармацевты где-то недоработали? И почему часто рекомендации из других стран отличаются противоположно от наших. Вот, например, известный в России справочник по лекарственным препаратам www.rlsnet.ru , созданный «Только для медицинских специалистов!», как написано на сайте.
В описании к телмисартану (ссылка на описание rlsnet.ru/tn_index_id_90213.htm) много чего не сходится. Например, читаю про побочные эффекты. Цитата: «Инфекции: нечасто — ….. частота неизвестна — сепсис, включая сепсис с летальным исходом».
«Хорошо», — подумал я и стал искать.
По запросу в PUBMED «sepsis telmisartan» был найден канадский обзор от 2014 года исследований «Антигипертензивные средства, действующие на ренин–ангиотензиновую систему и риск сепсиса» с 1 января 2000 г. по 30 июня 2009 г. Из когорты 550 436 больных гипертонической болезнью, 1965 пациентов были госпитализированы с сепсисом во время наблюдения (6,9 на 10 000 человек в год), из которых 824 умерли и у 346 развилась острая почечная недостаточность в течение 30 дней. Больные были госпитализированы с сепсисом в среднем в возрасте 76,6 ± 12,1 года. Цитата из исследования: «Compared with use of β-blockers, calcium-channel blockers or diuretics, use of ARBs, including telmisartan, was not associated with an elevated risk of sepsis (relative risk 1.09; 95% confidence interval 0.83-1.43)». То есть телмисартан, как и другие сартаны, не повышал риск сепсиса. А вот иАПФ немножко повышали риск сепсиса у очень пожилых людей, но не телмисартан.
Более того: «In comparison to hypertensive patients who had not been prescribed antihypertensive agents, the risk of sepsis was lower with current use of most classes of antihypertensive agents, but not with ACEI use.» То есть телмисартан, как и другие сартаны наоборот сокращали риск сепсиса в сравнении с гипертензивными пациентами, которые вообще не получали лечение препаратами для снижения давления.
Что получается? 6,9 пациентов, больных гипертонической болезнью, из 10 000 в год были госпитализированы из-за сепсиса, а фармацевты написали, что виноват в этом телмисартан? Ведь они пишут «Инфекции: нечасто — ….. частота неизвестна — сепсис, включая сепсис с летальным исходом».
Обратите внимание «НЕЧАСТО»
Классификация частоты развития побочных эффектов ВОЗ: очень часто (≥1/10); часто (от ≥1/100 до <1/10); нечасто (от ≥1/1000 до <1/100) редко (от ≥1/10000 до <1/1000); очень редко (<1/10000); частота неизвестна (не может быть оценена на основе имеющихся данных).
И по мнению фармацевтов виноват в этом телмисартан? А может быть просто, кто-то не особо напрягал себя и написал… на всякий случай…?
А теперь люди ведь читают. И больше всего обращают внимание на последние слова «включая сепсис с летальным исходом». И думают. «Ничего себе какой опасный препарат? Помереть от него можно». Соглашусь — звучит страшно.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/24803383
Стоит также вспомнить, что в многочисленных клинических исследованиях телмисартан, как и другие сартаны, показал себя очень безопасным:
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/18705533
- www.ncbi.nlm.nih.gov/pubmed/21633727
- www.ncbi.nlm.nih.gov/pubmed/19763608
Поискал дальше и стал смотреть на основании чего в описаниях препаратов делаются такие выводы. Нашел обоснования к такому описанию. Цитирую» Также стоит упомянуть, что в исследовании PRoFESSl, при приеме телмисартана наблюдались случаи сепсиса, по сравнению с плацебо. Данное заболевание могло иметь случайное происхождение или могло быть вызвано неизвестным в настоящее время механизмом». А вот цитата из оригинала этого исследования: «In this study, use of telmisartan was associated with a higher incidence of sepsis (0.70% vs 0.49%; re- lative risk 1.43, 95% CI 1.00, 2.06), including fatal cases (0.33% vs 0.16%; relative risk 2.07, 95% CI 1.14, 3.76), than placebo; this observation may be either a chance finding or related to an as yet unknown mechanism.[10]»
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/21504246
И что — это и есть доказательства? Учитывая, что никакие масштабные обзоры рисков не обнаруживают, а отдельные исследования только нашли связь, но не причину, которая может оказаться, как также заключают авторы» случайной. Это я о том, что связь не есть причина.
Предлагаем Вам оформить почтовую подписку на самые новые и актуальные новости, которые появляются в науке, а также новости нашей научно-просветительской группы, чтобы ничего не упустить.

Группа nestarenieRU в Facebook www.facebook.com/groups/nestarenie
Мой аккаунт в Facebook: https://www.facebook.com/nestarenieRU
YouTube-канал https://www.youtube.com/c/nestarenieRU
Знаете ли вы, что сайт nestarenie.ru — объективно один из самых популярных в России ресурсов про старение и долголетие — в Яндексе, в Гугле, по количеству, качеству и лояльности аудитории. nestarenie.ru имеет потенциал, чтобы стать одним из самых популярных сайтов о борьбе со старением не только в России, но и в мире. Для этого нужны деньги. Я призываю всех сделать пожертвования, а также убедить своих друзей поступить аналогично.
-
-
- Карта Viza (доллары): 4215 8901 1587 0138 для переводов за пределами РФ
- Карта МИР в Сбере (рубли): 2202 2032 1501 6686 (МАЙЯВИ Ч.) — на территории РФ
-
Узнайте подробнее помочь развитию блога.
Рекомендуем ещё почитать следующие статьи:
- Метформин — самое изученное и надёжное лекарство от старости.
- Подробная программа продления жизни научно доказанными способами.
- Витамин K2 (МК-7) сокращает смертность
- Витамин B6+магний снижают смертность на 34%
- Глюкозамин Сульфат эффективно продлевает жизнь и защищает от многих видов рака
- Фолаты для предупреждения раннего старения
- Как победить метилглиоксаль — вещество, которое нас старит.
Инструкция к лекарству является важным информационным средством для тех, кто хочет его принимать. Опрос показывает, что все еще имеется много пациентов, которые, несмотря на наличие инструкции, чувствуют себя, тем не менее, скорее неуверенными, чем хорошо проинформированными об употреблении данного лекарства. По оценкам органов здравоохранения от 16 до 25 тысяч людей в стране ежегодно умирает от тех или иных лекарств. Еще больше тех людей, которые должны лечиться в больнице от тяжелых последствий употребления лекарств.
Содержание инструкции к лекарству
Наименование лекарственного препарата: Дополнение «comp» или «plus» после названия лекарства указывают на то, что в соответствующем препарате содержится комбинация из многих веществ, а дополнение «mono», наоборот, что содержится только одно вещество. Дополнения «forte» (сильное, высоко дозированное) и «mite» (среднее, обычно наполовину от «forte» дозированное) содержат в себе информацию на уровень содержания вещества, а цифры, например, 200 или 400, — на массу вещества в условной единице лекарственного препарата. Обозначения «retard» или «depot» находятся в названии препарата, вещество которого освобождается из организма человека медленно или замедленно, например, только через день.
Состав препарата (Zusammensetzung): в нем указывается вещество на одну таблетку, капсулу, ампулу, драже, 100 грамм мази или 100 миллилитров раствора или сока.
Другие составные части препарата (WeitereBestandteile): Здесь содержится перечень вспомогательных веществ, знание которых может играть важную роль для пациентов, реагирующих на них в виде аллергии к ним.
Форма подачи препарата (Darreichungsform): В таблетках, драже, капсулах, ампулах, каплях, сиропе, мази, геле и в других разнообразных формах и видах.
Область применения или индикация препарата (Anwendungsgebieteили Indikation): Указываются болезни, при лечении которых препарат действует успешно. Этот перечень болезней, конечно, далеко не всегда полный, поэтому данный препарат должен употребляться по совету врача в том случае, когда болезнь, которой страдает пациент, не находится в указанной области применения.
Противопоказания (Gegenanzeigen): Здесь важно обратить внимание на то, имеются ли в этом разделе указания на определенные обстоятельства или болезни пациента. Если таковые имеются в этом перечне, то необходимо обсудить это с лечащим врачом. Применение препарата в таком случае должно осуществляться с учетом категорических указаний врача.
Указания предупредительного характера или меры предосторожности при употреблении препарата (Warnhinweise / VorsichtsmaßnahmenfürdieAnwendung): При применении многих лекарств существуют определенные особенности: например, препарат, содержит алкоголь, поэтому его не могут принимать дети и беременные женщины. Данный препарат может также вести к нежелательным реакциям пациента, поэтому, например, активные участники дорожно-транспортного движения должны избегать его употребления.
Побочные действия препарата (Nebenwirkungen): Данный большой раздел инструкции содержит возможные побочные воздействия препарата на пациента, но которые при этом чаще всего могут возникнуть у него с весьма низкой долей вероятности. В Германии, допускаемые к употреблению лекарственные препараты имеют т.н. положительное соотношение для качественной пары польза-риск (Nutzen-Risiko-Verhältnis). Многие описанные в этом разделе побочные действия или полностью безвредны или весьма редко наблюдаются. Так, препарат может причинить, например, часто («häufig») головокружение, что означает на деле, что в одной сотне случаев его применения только не более чем у 9 пациентов это может произойти. Ну, а редкие («seltene») побочные действия означают, что они наблюдаются только у одного из тысячи пациентов. Тем не менее, тот , кто принимает данный препарат, должен тщательно наблюдать за физическими, умственным и психическими изменениями своего организма. Обо всех явлениях (например, сыпи на коже, головной боли, тошноте, поносе, головокружении, повышении температуры, усталости, колебаниях настроения, перевозбудимости и т.д.) следует сразу же сообщить своему лечащему врачу. Ведь речь может в этом случае идти не только о непереносимости, но и о симптомах другой болезни.
Взаимодействие препарата (Wechselwirkungen): Когда два лекарственных препарата (например, лекарство и продукт питания) взаимно влияют на организм человека, то говорят о взаимодействии или также об интеракции лекарства. Эти интеракции могут сказываться на организме различными способами, при которых они усиливают или ослабляют действие препарата. Это обстоятельство следует точно проверить. При сомнении — посоветоваться с аптекарем. Ну, а лечащий врач должен проинформировать пациента по поводу приема других лекарств.
Указание к дозировке препарата (или вид и продолжительность применения лекарства) — Dosierungsanleitung / ArtundDauerderAnwendung: В этом разделе можно прочитать о том, как, когда, где, сколько, как часто и как долго можно принимать или употреблять данный препарат. В случае если лечащий врач предписывает другую дозировку, то следует соблюдать его указание.
Ошибки при применении препарата и передозировка его (Anwendungsfehlerund Überdosierung): В этом разделе говорится о том, что делать том случае, когда пациент забыл вовремя принять лекарство или по ошибке принял двойную его дозу.
Указания и данные о хранении препарата (HinweiseundAngabenzurHaltbarkeit): В этом разделе содержатся указания по срокам и условиям сохранения лекарства и продолжительности его употребления. Так, глазные капли должны использоваться не дольше 4 — 6 недель после открытия бутылочки с ними. Некоторые лекарства такие, как инсулин, должны храниться в холодильнике, другие – быть защищены от света. Лекарства, срок хранения которых истек, вообще нельзя употреблять.
Важные советы
- Спросите у лечащего врача, почему он назначил вам именно данное лекарство. При приобретении лекарства в аптеке не стесняйтесь выяснить подробно все, что относится к употреблению данного препарата. А инструкция к нему может служить вам в порядке перестраховки.
- Уходите из врачебного праксиса только тогда, когда вы точно знаете, как применять назначенный вам препарат: дозу, время приема и особые условия употребления. А указания инструкции должны вам служить только в качестве напоминания об этом. Если вы не уверены точно в чем-то, не стесняйтесь переспросить об этом врача или аптекаря прежде, чем вы станете применять препарат в течение длительного времени.
- В каждом случае выясните у лечащего врача или аптекаря о побочных действиях назначенного вам лекарства, нежелательных его последствиях для организма, смешивании его с другими лекарственными препаратами и его непереносимости, даже если эти факторы проявляются у вас кратковременно. Врачи и аптекари сообщат об этом соответствующим государственным ведомствам, которые в случае частых сообщений подобного рода примут необходимые меры безопасности. Поэтому вы должны сохранять упаковку и инструкцию к препарату до окончания его употребления.
- В период приема лекарственного препарата ни в коем случае нельзя употреблять алкоголь. Поговорите с лечащим врачом тогда, когда у вас с этим возникают некоторые проблемы.
- Тщательно предохраняйте лекарства от попадания их в руки детей!
О рисках и побочных действиях лекарств
С помощью правильных дозировок лекарства должны помогать лечить болезни, хотя многие пилюли человек принимает нередко без врачебного назначения и даже не зная, как данные таблетки переносятся с другими, назначенными врачом лекарствами. А иногда, наоборот, просто отказывается от каких-то таблеток, потому что в инструкции к лекарству указывается на слишком сильные его побочные действия. Это может быть опасным, разъясняет д-р Томас Дитц (Dr. ThomasDietz).
Прежде чем лекарственный препарат поступает в немецкую аптеку, тщательно проверяется с помощью соответствующей пройедуры допуска его к применению, каково фактически оно оказывает основное воздействие и каковы, а, главное, в каком объеме, оно обладает нежелательными побочными действиями. Следует иметь в виду, что практически не существует активно действующее лекарство без риска возможных его побочных действий. По-другому дело обстоит с продуктами, которые можно найти в аптекарско-химическом магазине (Drogeriе) или в обычных универсальных магазинах и которые вроде бы нередко подобны лекарственным препаратам, продающимися в аптеках. Они также обещают лечебный или содействующий здоровью эффект, но не проходили процедуру допуска их в качестве лекарственного средства. Они обозначаются в качестве дополняющих питание средств. Однако их эффективность весьма спорна. Как правило, их спектр действия удостоверяют частные институты, правда, указывая при этом на возможные осложнения при неправильной дозировке.
Инструкция к лекарству: непонимание вызывает страх его применения
Такая инструкция, которая нередко совершенно неправильно называют рекламой лекарства, является обязательным приложением к лекарственному препарату. Прочитает ли ее на самом деле потребитель и поймет ли ее, это уже другой вопрос. Дело в том, что многие люди не настолько хорошо владеют языком, чтобы точно понять инструкцию к лекарству, и поэтому у них складывается впечатление, что такая инструкция содержит информацию главным образом не для пациента, а в основном для врачей и аптекарей. Но у врача обычно нет времени прочитать и так разъяснить инструкцию своему пациенту, чтобы у него не осталось никаких неясностей в отношении применения лекарства. Но и в аптеке обычно обстоит дело таким же образом. Нередко такая ситуация ведет к тому, что пациент прежде всего обращает внимание на раздел побочные действия и взаимодействия с другими лекарствами и не разобравшись по существу в нем, начинает испытывать сильный страх в части применения данного лекарства и поэтому нередко либо вообще отказывается от его применения, либо произвольно существенно уменьшает его дозировку. При этом ему кажется, что таким образом он избегает побочных действий назначенного ему лекарства, не снижая его основного эффекта. На самом деле такое поведение испуганного пациента затрудняет, конечно, достижение обещанного эффекта при лечении болезни. Помочь в этом случае может лишь четкое указание на частоту возникновения возможных побочных действий, причем далеко не каждое упомянутое в соответствующем разделе инструкции действие вообще может проявиться или практически гораздо реже, чем даже на это указывается.
Как часто следует ожидать побочных действий?
Рядом с перечнем побочных действий в инструкции указываются, с какой частотой они могут наступать. Так что же эти цифры означают?
- Очень редко: т.е. меньше чем 0,01% случаев (иначе говоря, только у одного пациента из 10 тысяч);
- Редко: т.е. в худшем случае у одного пациента из тысячи, а в лучшем случае – у одного пациента из 10 тысяч;
- Случайно: т.е. в худшем случае у одного пациента из ста, а в лучшем случае – у одного пациента из тысячи;
- Часто: т.е. в худшем случае у одного пациента из десяти, а в лучшем случае – у одного пациента из ста;
- Очень часто: чаще, чем у 10% пациентов, которые лечатся с помощью данного лекарства. Кроме того, изготовитель должен назвать отдельные случаи, которые прежде не были охвачены статистическим учетом.
Принимайте лекарства вовремя
Дальнейшее замешательство может вызвать у пациента указания как и когда следует принимать лекарство. После того, как вы проглотили таблетку, ее вещество усваивается через тонкий кишечник и только тогда может проявить свое действие. Некоторые продукты питания оказывают существенное влияние на возможности лекарственного препарата, например, сок грейпфрута, молочные продукты, чай, кофе, алкоголь и т.д. Поэтому рекомендуется избегать соответствующих комбинаций лекарства с некоторыми продуктами питания. Этому служат указания о способе и виде приема лекарства:
- Перед едой: по крайне мере, за полчаса, а лучше за час до еды;
- Во время еды: самое позднее, через пять минут после окончания еды;
- После еды: по крайне мере, через полчаса, а лучше через час после еды.
Точная дозировка лекарства
Для успешного лечения действует следующее правило: лекарственные препараты следует по возможности принимать в точном количестве и через точные интервалы времени согласно предписанию врача. Только таким образом лечение данным препаратом может протекать в желаемом русле. Если же появляются побочные явления, которые больше не оправдывают дальнейшее лечение именно данным лекарством, то задача лечащего врача подобрать ему подходящую альтернативу. Это удается лучше тогда, когда ясно, что неудовлетворительные результаты имеют место не из-за того, что пациент принимал лекарство рекомендуемыми врачом дозами и через соответствующие интервалы времени.
Составитель: Толстоног Веньямин
Источник http://www.daserste.de/moma/servicebeitrag_dyn~uid,zweh4hs2bc20g65b~cm.asp